Introduction
Les événements thromboemboliques, notamment la thromboembolie veineuse (profonde) ou la thromboembolie artérielle, sont rares chez les enfants comparativement à la population adulte. La grande majorité des enfants atteints d’une thrombose présente une ou plusieurs affections médicales sous-jacentes associées (telles qu’une infection, une tumeur maligne, une maladie grave et/ou la présence d’un cathéter veineux central [CVC]) au moment de l’événement. Contrairement aux adultes, la thrombose spontanée représente une complication très rare(1-4). Étant donné que la thrombose chez les enfants survient généralement chez des enfants malades, la présence d’une thrombophilie constitue probablement un facteur de risque supplémentaire plutôt qu’une cause isolée de thrombose(3).
Marqueurs de thrombophilie en laboratoire
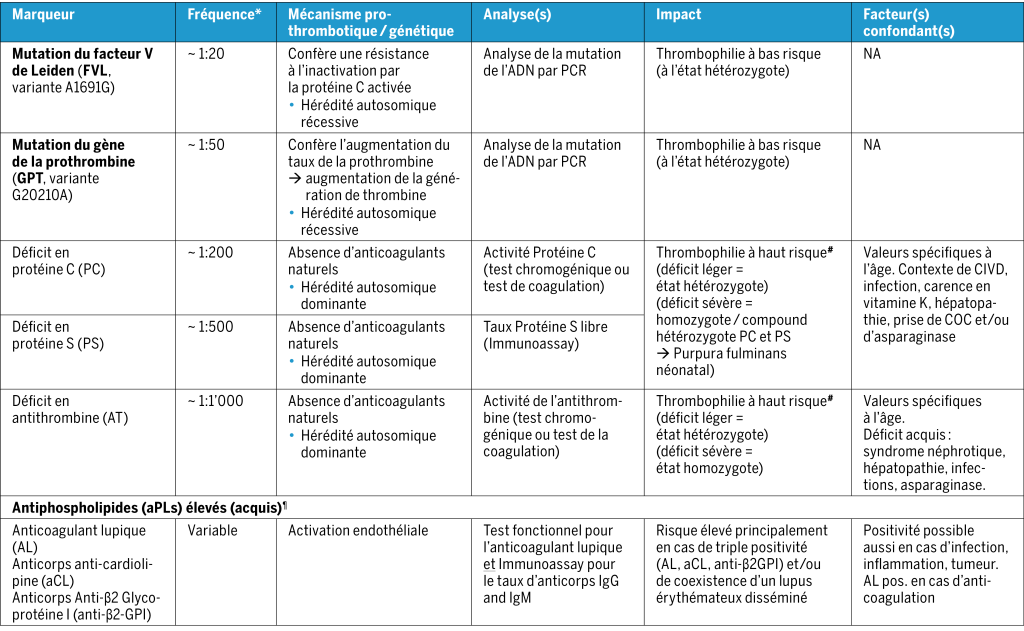
La thrombophilie indique la propension à former des caillots sanguins qui peut résulter de facteurs de risque héréditaires et/ou acquis. Le dépistage de la thrombophilie fait généralement référence à l’analyse en laboratoire de marqueurs d’hypercoagulabilité potentiellement associés à un risque accru de thrombose. Un certain nombre de marqueurs de thrombophilie héréditaire et acquise ont été identifiés. Les marqueurs de la thrombophilie héréditaire comprennent la mutation prothrombotique dans les gènes codant le facteur V (mutation facteur V Leiden, FVL, variante G1691A) et la prothrombine (mutation du gène de la prothrombine, GPT, variante G20210A) et les déficits en anticoagulants naturels, notamment l’antithrombine (AT), la protéine C (PC) et la protéine S (PS)(3-5,8). Les affections acquises impliquent les anticorps antiphospholipides (aPLs). Le dépistage des aPLs doit être inclus dans le cadre d’une thrombose et/ou d’autres caractéristiques cliniques suggérant un syndrome des antiphospholipides (APS) chez le cas index(3,5,9).
D’autres facteurs de risque de thrombose basés sur des analyses de laboratoire ont été décrits, mais aucun n’a été largement accepté. Il s’agit plus précisément de l’augmentation des facteurs de coagulation (en particulier le facteur VIII)(10), de l’homocystéine et/ou de la lipoprotéine a(5). Cependant, leur importance dans le risque de complications thromboemboliques chez les enfants reste incertaine et nous suggérons de ne pas effectuer ces tests de manière systématique lors de l’évaluation de la thrombophilie chez les enfants, car il n’existe pas de recommandations sur la manière dont des résultats anormaux devraient influencer la prise en charge de ces patient·e·s(3). Le dépistage des mutations (polymorphismes) de la méthylène tétrahydrofolate réductase (MTHFR) ne devrait plus être inclus dans les panels de thrombophilie(11).
Les marqueurs du panel de dépistage de la thrombophilie, leur mécanisme d’action, leur analyse et d’autres caractéristiques sont détaillés dans le tableau 1. La fréquence rapportée de chaque trait thrombophilique dans la population générale, comme illustrée dans le tableau 1, peut varier en fonction du type de marqueur (de 5 % pour la mutation FVL à 1:1000 pour le déficit en AT) et en partie en fonction de l’origine ethnique de la population(3, 5, 12, 13).
L’influence potentielle de la présence d’un trait de thrombophilie sur le risque de développer une première thrombose veineuse, une récidive, un accident vasculaire cérébral (AVC) ischémique, ou d’une thrombose artérielle périphérique (non-cérébrale) chez l’enfant a été partiellement étudiée et rapportée(4,14-19). Dans l’ensemble, le risque d’un premier évènement thrombotique veineux, ou récurrent, était le plus élevé chez les personnes présentant un déficit en AT, PC ou PS et/ou des mutations homozygotes/hétérozygotes composites de FVL ou PG (trait thrombophilique à haut risque). En revanche, les hétérozygotes pour la mutation FVL ou PG présentaient un risque plus faible (trait thrombophilique à faible risque)(3,20). Pour l’AVC ischémique chez les enfants, mais pas pour l’AVC ischémique périnatal, la prévalence d’un trait de thrombophilie était plus élevée que dans le groupe témoin(21-23). L’impact de la présence de marqueurs de thrombophilie dans les événements thromboemboliques artériels non-cérébraux est moins clair(4).
Démarche pour le dépistage de la thrombophilie
Les événements thromboemboliques en âge pédiatrique surviennent principalement chez des enfants malades hospitalisés. Leur prise en charge, y compris toute décision relative aux tests de thrombophilie, implique souvent des médecins hospitaliers. D’autre part, les pédiatres en cabinet peuvent être sollicités par les parents pour obtenir des conseils sur la marche à suivre en cas d’antécédents familiaux d’événements thromboemboliques et/ou de thrombophilie, dans le cadre d’une consultation ambulatoire. Idéalement, ils devraient orienter le·la patient·e et sa famille vers un hématologue pédiatrique afin d’obtenir des conseils avisés avant d’effectuer le dépistage(3). En effet, les recommandations relatives au dépistage de la thrombophilie chez les enfants et les adolescent·e·s, compte tenu des données disponibles limitées, se basent majoritairement sur l’avis d’expert·e·s. Elles doivent donc faire l’objet d’une discussion au cas par cas lors d’une consultation spécialisée.
Dans l’ensemble, les scénarios dans lesquels un dépistage de la thrombophilie chez les enfants peut rentrer on considération comprennent(1, 24) :
- les patient·e·s pédiatriques ayant déjà présenté un événement thrombotique (cas index) et
- les enfants/adolescent·e·s non affecté·e·s (asymptomatiques) ayant, ou pas, des antécédents familiaux positifs de thrombose (surtout apparentés de premier degré).
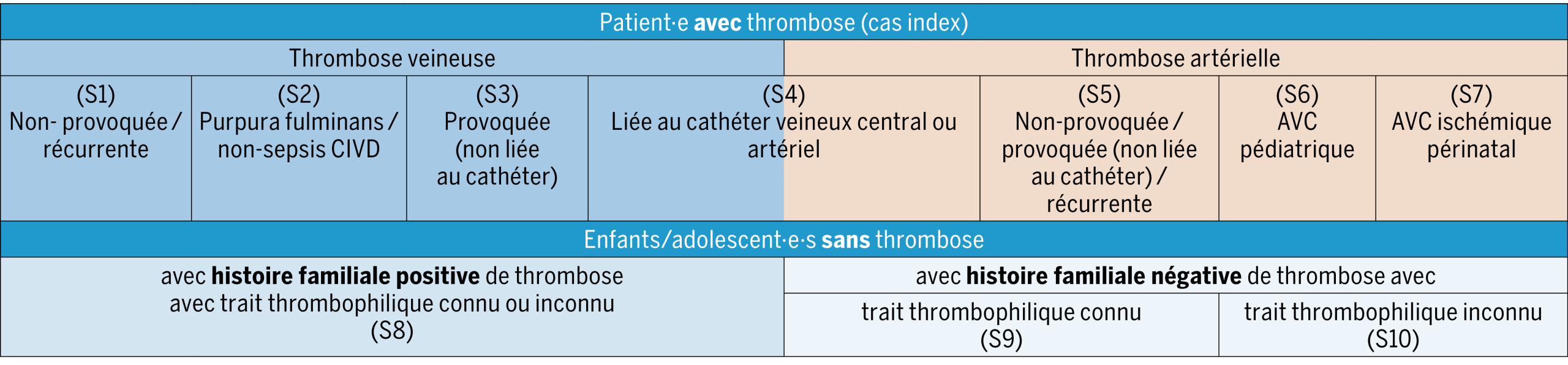
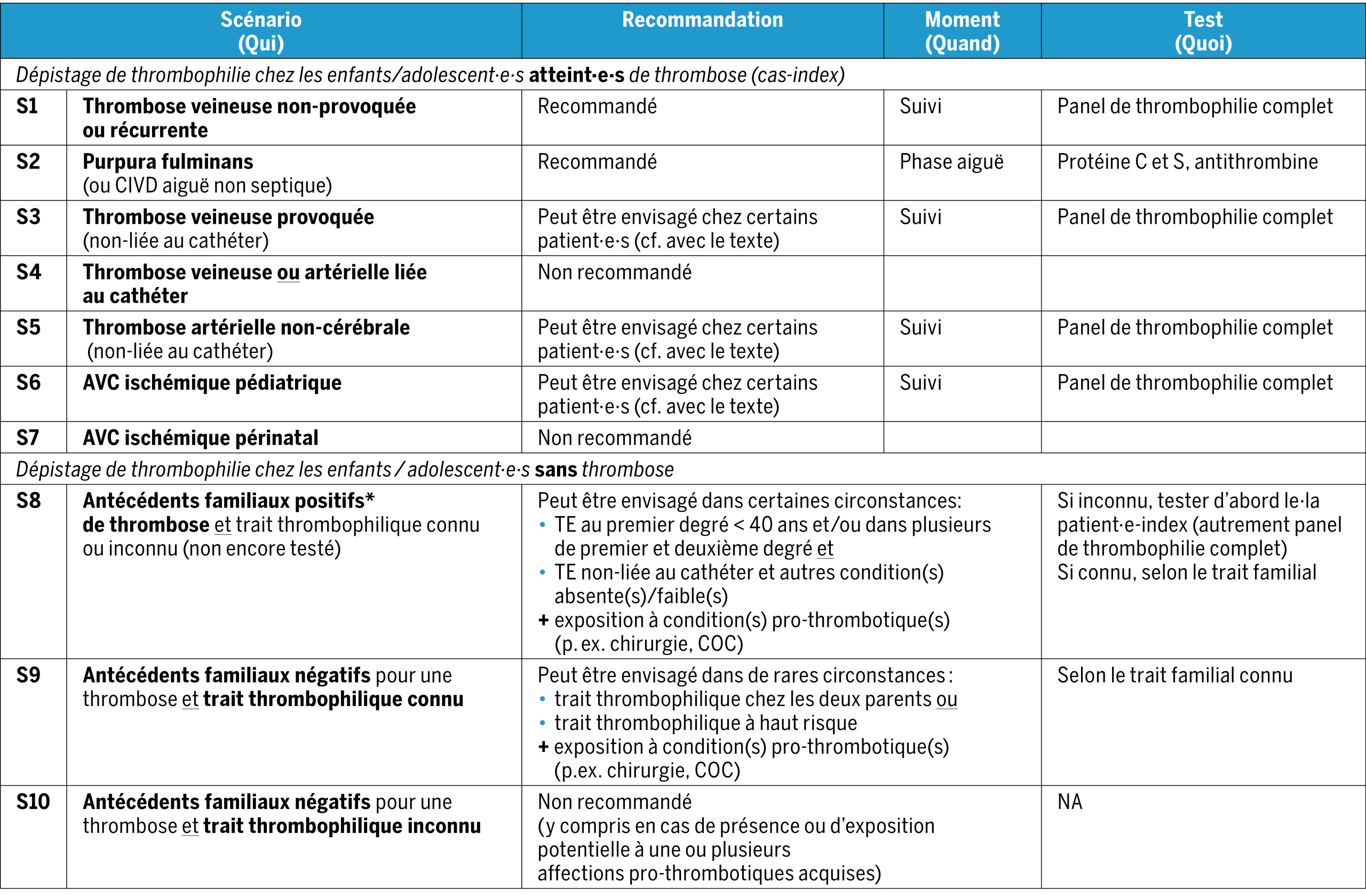
L’évaluation se concentre sur trois aspects principaux. En premier lieu, il s’agit de déterminer l’utilité du dépistage dans un contexte spécifique (qui). En deuxième lieu, il conviendra de déterminer le moment opportun pour sa mise en œuvre (quand). Dans l’éventualité où cela s’avérerait indispensable, il conviendrait de spécifier le ou les tests à effectuer (quoi). Une vue d’ensemble indicative des scénarios (S1 à S10) et des recommandations lors du dépistage est présentée dans la figure 1, le tableau 2 et ci-dessous.
Des possibles arguments en faveur de l’établissement d’un bilan de thrombophilie peuvent inclure :
- meilleure compréhension de la physiopathologie de l’évènement ;
- évaluation individuelle du risque de récidive ;
- sensibilisation à la thromboprophylaxie pharmacologique lors de situations à haut risque (chirurgie, maladie grave, traumatisme);
- orientation sur l’usage de contraceptifs oraux combinés.
D’autre part, il faudrait considérer aussi comme possibles arguments en défaveur d’un dépistage :
- rareté de la thrombose pédiatrique, le plus souvent liée à des facteurs acquis;
- prophylaxie secondaire déjà indiquée en cas de risque clinique connu;
- risque de mauvaise interprétation des résultats ou de fausse réassurance;
- information familiale possible sans tests supplémentaires;
- enjeux éthiques des tests génétiques chez l’enfant, réservés aux situations où une intervention précoce améliore le pronostic(3, 25)
A noter que tout résultat anormal de test non basé sur l’ADN (y compris les protéines C et S et l’antithrombine) qui pourrait être altéré en raison de l’âge de l’enfant et/ou de la présence d’autres affections acquises (voir tableau 1) doit être confirmé. En outre, il est conseillé de tester les deux parents avant de conclure à la présence d’un déficit héréditaire en protéine C, protéine S ou antithrombine.
Dépistage de thrombophilie chez les patient·e·s ayant subi·e un événement thromboembolique (cas index) :
La prévalence rapportée des différents traits de thrombophilie chez les patient·e·s pédiatriques atteint·e·s de thrombose peut varier entre 13 et 79 %, ce qui reflète principalement l’hétérogénéité de la conception des études, ainsi que les caractéristiques cliniques et démographiques des populations étudiées(3). Il est essentiel de comprendre les circonstances dans lesquelles l’évènement thrombotique s’est produit afin de mettre en perspective l’impact que les résultats du test de thrombophilie peuvent éventuellement avoir sur la prise en charge.
Vous trouverez ci-dessous des conseils pour le test de thrombophilie basés sur différents scénarios (S1-7) chez les patient·e·s atteint·e·s de thrombose (figure 1, table 2) :
- Pour la thrombose veineuse non-provoquée ou récurrente chez les nouveau-nés, les enfants et les adolescent·e·s (S1), il est recommandé de réaliser un test diagnostique de thrombophilie. Rationnel : les thromboses veineuses non provoquées (spontanées) sont extrêmement rares en pédiatrie, et leur taux de récidive dans ce contexte est relativement élevé et peut être influencé par une thrombophilie sous-jacente(3, 14, 19, 26). La thrombophilie héréditaire était plus fréquente chez les enfants plus âgés présentant une TEV non-provoquée (60 %) que chez les enfants présentant une TEV secondaire à une affection médicale sous-jacente (<10%)(12). Les résultats peuvent aider à prendre une décision concernant la durée du traitement et, éventuellement, la nécessité de dépister les membres de la famille, principalement dans le contexte d’un trait thrombophilique à haut risque (définition cf. partie introduction) .
- Pour les nouveau-nés atteints de purpura fulminans (S2) (ou d’autres thromboses graves non-provoquées telles que des thromboses des sinus veineux cérébraux étendues), il est fortement recommandé de procéder immédiatement à des tests de thrombophilie afin de détecter un trait de thrombophilie à haut risque et plus particulièrement un déficit sévère (homozygote/compound hétérozygote) en protéines S, C et antithrombine. Rationnel : un traitement substitutif doit être instauré rapidement(27, 28). Dans de tels cas, il est fortement recommandé de consulter un centre spécialisé dans le traitement de la thrombose.
- En cas de thrombose veineuse provoquée (non-liée à un CVC) (S3) chez les nouveau-nés, les enfants et les adolescent·e·s, le dépistage de thrombophilie n’est généralement pas proposé, mais peut être considéré dans certains circonstances. Rationnel : les données en matière sont très limitées et les pratiques peuvent varier. Chez les patient·e·s présentant une première thrombose veineuse associée à une condition/circonstance claire (par exemple, infection systémique grave, cancer/traitement associé, chirurgie majeure/traumatisme, syndrome néphrotique), le dépistage n’est pas recommandé. Ceci sur la base aussi que les facteurs déclenchants sont dans la plus part des cas transitoires et que la durée de traitement pour une thrombose veineuse provoquée est en général ≤ 3 mois(1). Cependant, il peut être raisonnable d’effectuer des tests de thrombophilie dans certaines circonstances, telles que l’événement thrombotique inhabituel et/ou l’incertitude/faiblesse du ou des facteurs déclenchants(14, 20).
- Pour une thrombose veineuse ou artérielle liée à un CVC ou à un cathéter artériel (CA), respectivement, (S4) chez les nouveau-nés, les enfants ou les adolescent·e·s, les tests de thrombophilie ne sont pas recommandés. Rationnel : la présence du cathéter est le facteur de risque le plus important de thrombose chez les enfants, et les tests de thrombophilie ne jouent aucun rôle supplémentaire dans l’orientation des décisions thérapeutiques(4, 29, 30).
- Pour les thromboses artérielles non-cérébrales non-provoquées ou provoquées (non-liées à un cathéter) (S5), un dépistage peut être envisagé en cas d’événement thrombotique inhabituel et/ou d’incertitude concernant le ou les facteurs déclenchants. Rationnel : cette complication est rare et associé comme complication lors de certaines maladies, comme lors d’une malformations vasculaires, certains formes d’artérites (p.ex. Kawasaki, artérite de Takayasu) ou hyperlipidémie familiale. De plus seules des données marginales sont disponibles, ce qui ne permet pas de formuler une recommandation définitive(2, 4).
- Pour l’accident vasculaire cérébral (AVC) ischémique pédiatrique (S6), un dépistage de la thrombophilie (à l’exception des enfants atteints de drépanocytose) peut être envisagé chez certain·e·s patient·e·s en fonction des circonstances de son apparition(21, 31). Rationnel : les données actuelles suggèrent un lien entre la présence d’une thrombophilie diagnostiquée en laboratoire (héréditaire ou acquise) et l’apparition d’un AVC ischémique(18). Néanmoins, ces données ne sont pas suffisantes pour valider l’utilité de ces tests, compte tenu de la diversité des contextes dans lesquels l’AVC peut survenir. De plus, l’impact de la thrombophilie sur le risque de récidive de l’AVC est moins clair(17, 18, 21, 31).
- Pour les AVC ischémiques dans la période périnatale (S7), les tests de thrombophilie ne sont pas recommandés. À l’heure actuelle, aucune preuve ne justifie la réalisation systématique de ces tests en dehors des protocoles de recherche. L’importance de la thrombophilie dans la physiopathologie et les résultats à long terme des AVC périnataux n’est pas encore connue(23,32).
Le moment auquel effectuer les tests doit être déterminé en fonction de leur potentiel impact sur les soins prodigués à l’enfant. À quelques exceptions près, les tests de thrombophilie ne sont pas recommandés en cas d’événement thrombotique aigu. En effet, les résultats de ces tests influencent rarement la prise en charge aiguë d’un·e patient·e atteint·e de thrombose, qui doit être traitée indépendamment. Les exceptions concernent les nouveau-nés présentant un purpura fulminans (déficit sévère en protéine S), pour lesquels un traitement de substitution doit être mis en place rapidement(27, 28). En outre, en cas de forte suspicion d’APS, il convient d’envisager de tester les aPL avant de commencer l’anticoagulation, car cela modifierait l’analyse.
Dans la plupart des cas, le dépistage, si retenu comme indiqué, doit être reporté au plus tôt à 3 à 6 mois et après l’arrêt du traitement anticoagulant. Les résultats peuvent aider à estimer le risque de récidive et guider la durée du traitement ou la prophylaxie secondaire lors de situations à risque.
Toutefois, les données disponibles ne permettent pas encore de proposer aux patient·e·s et à leurs proches une approche définitive fondée sur le risque(1).
Dépistage de thrombophilie chez les patient·e·s sans antécédent de thrombose (patient·e·s asymptomatiques) :
La décision de procéder ou non au dépistage dans ce contexte repose davantage sur la présence ou non d’antécédents familiaux positifs de thrombose, et dans une moindre mesure, sur la présence d’un trait thrombophilique positif dans la famille.
Dépistage chez les enfants/adolescent·e·s avec des antécédents familiaux positifs de thrombose (S8) :
Pour les enfants/adolescent·e·s ayant des antécédents familiaux positifs de thrombose avec un trait de thrombophilie connu ou inconnu (non encore testé), le dépistage n’est pas systématiquement recommandé, mais peut être envisagé dans certaines circonstances. Rationnel : Les données sur la prévalence de la thrombose (principalement la thrombose veineuse) chez les enfants ayant des antécédents familiaux positifs et sur la présence d’un trait de thrombophilie dans ce contexte sont limitées et dérivent principalement des données des adultes(3, 20).
Bien que controversé, le dépistage peut être raisonnable dans certaines situations, notamment en cas d’antécédents familiaux, tels qu’une thrombose non-liée au cathéter et associée à des facteurs déclenchants faibles (comme p.ex. la pilule) ou non identifiés, survenant chez un parent du premier degré avant l’âge de 40 ans, ou chez plusieurs parents proches. Il est donc très important d’élucider les circonstances dans lesquelles la thrombose est survenue chez le ou les patient·e·s index de la famille, notamment les facteurs de risque, les conditions et l’âge au moment de la complication thrombotique. En autre, la thrombose veineuse est plus fréquente chez les porteurs·euses d’une thrombophilie, en particulier d’un déficit en antithrombine, protéine C ou protéine S (incidence annuelle : 2.82 %), plutôt que pour les traits à faible risque (FVL ou PTG hétérozygotes, 0.2–0.5 %/an)(3, 14, 15). Par conséquent, en ce qui concerne le dépistage, si retenu indiqué, il devrait d’abord être effectué chez les patient·e·s index et puis chez les membres de sa famille asymptomatiques n’ayant pas présenté de complication thrombotique et surtout afin d’identifier un trait à haut risque.
Chez les enfants/adolescent·e·s sans antécédents familiaux de thrombose :
- Avec un trait de thrombophilie connu dans la famille, le dépistage n’est pas à priori recommandé (S9) et peut être envisagé dans de rares circonstances. Rationnel : L’incidence absolue de la thrombose chez les enfants présentant un trait de thrombophilie, surtout à faible risque (mutation hétérozygote FVL ou PTG), reste très basse. Toutefois, même si le consensus n’est pas unanime parmi les expert·e·s, le dépistage peut être envisagé dans certaines circonstances, telles que : en présence de marqueurs de thrombophilie à haut risque (voir ci-dessus) et/ou la présence d’un trait de thrombophilie chez les deux parents (avec un risque de trait de thrombophilie homozygote ou hétérozygote composé chez les descendants) et dans le contexte de possible exposition à risque thrombotique. Par exemple, avant l’administration de COC, il peut être envisagé de dépister les filles issues de familles présentant un trait de thrombophilie à haut risque, afin d’éviter l’utilisation de contraceptifs contenant des œstrogènes en cas de résultat positif. Il est toutefois préférable de reporter le dépistage jusqu’à ce qu’ils soient en âge de décider eux-mêmes, après avoir pesé le pour et le contre(3, 20).
- Sans trait de thrombophilie connu, le dépistage n’est pas recommandé dans ce cas (S10). Rationnel : aucun essai clinique ne démontre l’efficacité et le rapport bénéfice/risque d’une thromboprophylaxie ni le bénéfice par rapport à la décision d’introduire une COC(5).
Globalement, en ce qui concerne le moment approprié pour procéder (si vraiment retenu nécessaire) au dépistage, il semble raisonnable de le reporter chez les enfants asymptomatiques jusqu’à ce qu’ils soient en âge de décider par eux-mêmes après avoir pesé le pour et le contre, étant donné que l’incidence absolue de la thrombose en âge pédiatrique est très faible, même chez les enfants avec trait de thrombophilie. En effet, un dépistage dans ce contexte peut ne pas être justifié au vu des avantages et des inconvénients mentionnés auparavant(3). Les tests chez les enfants asymptomatiques ne doivent être effectués que pour les thrombophilies génétiques bien établies, qui sont résumées dans le tableau 1. Si le trait de thrombophilie familiale est inconnu, il faut d’abord envisager de tester le membre de la famille index avec TE. En cas de trait de thrombophilie connu, il est conseillé d’effectuer ce test de manière sélective.
Conclusion
Les complications thrombotiques chez les enfants restent rares et surviennent majoritairement en présence de plusieurs facteurs de risque/conditions concomitants au moment de la complication. La présence d’une thrombophilie constitue probablement un facteur de risque supplémentaire plutôt qu’une cause isolée de thrombose(3). Il incombe au médecin traitant de décider si, quand et quels tests sont appropriés pour chaque enfant, et dans tous les cas, il est conseillé que le dépistage de thrombophilie fasse l’objet d’une discussion approfondie avec le·la patient·e et sa famille et qu’il soit proposé en consultation avec le spécialiste.
Références
- Monagle P, Azzam M, Bercovitz R, Betensky M, Bhat R, Biss T, et al. American Society of Hematology/International Society on Thrombosis and Haemostasis 2024 updated guidelines for treatment of venous thromboembolism in pediatric patients. Blood Adv. 2025;9(10):2587-2636.
- Rizzi M, Albisetti M. Treatment of arterial thrombosis in children: Methods and mechanisms. Thromb Res. 2018;169:113-119.
- Nowak-Gottl U, van Ommen H, Kenet G. Thrombophilia testing in children: What and when should be tested? Thromb Res. 2018;164:75-78.
- Rizzi M CAK, Bosch A., Albisetti M Arterial Thrombosis. In: Blanchette VS BL, Carcao MD, Kumar R, Rand ML, Revel-Vilk S editor. SickKids Handbook of Pediatric Thrombosis and Hemostasis, ed 3, rev and ext S.Karger AG, Basel; 2024. p. pp275-287.
- Sabapathy C. AA, Kumar R., Avila L., Van Ommen C.H. Diagnostic Approach to Thrombosis and Thrombophilia In: Blanchette VS BL, Carcao MD, Kumar R, Rand ML, Revel-Vilk S editor. SickKids Handbook of Pediatric Thrombosis and Hemostasis (3rd, revised and extended edition): S.Karger AG, Basel; 2024. p. 233–255.
- Kumar R, Bakeer N, Dawson J, Al-Mughairy A, Stanek J, Dunn A, et al. Impact of SERPINC1 mutation on thrombotic phenotype in children with congenital antithrombin deficiency-first analysis of the International Society on Thrombosis and Haemostasis pediatric antithrombin deficiency database and biorepository. J Thromb Haemost. 2023;21(5):1248-1257.
- Marlar RA, Gausman JN, Tsuda H, Rollins-Raval MA, Brinkman HJM. Recommendations for clinical laboratory testing for protein S deficiency: Communication from the SSC committee plasma coagulation inhibitors of the ISTH. J Thromb Haemost. 2021;19(1):68-74.
- Cooper PC, Pavlova A, Moore GW, Hickey KP, Marlar RA. Recommendations for clinical laboratory testing for protein C deficiency, for the subcommittee on plasma coagulation inhibitors of the ISTH. J Thromb Haemost. 2020;18(2):271-277.
- Vandevelde A, Chayoua W, de Laat B, Moore GW, Musial J, Zuily S, et al. Added value of antiphosphatidylserine/prothrombin antibodies in the workup of thrombotic antiphospholipid syndrome: Communication from the ISTH SSC Subcommittee on Lupus Anticoagulant/Antiphospholipid Antibodies. J Thromb Haemost. 2022;20(9):2136-2150.
- Bosch A, Uleryk E, Avila L. Role of factor VIII, IX, and XI in venous thrombosis recurrence risk in adults and children: A systematic review. Res Pract Thromb Haemost. 2023;7(2):100064.
- Deloughery TG, Hunt BJ, Barnes GD, Connors JM, Committee WTDS. A call to action: MTHFR polymorphisms should not be a part of inherited thrombophilia testing. Res Pract Thromb Haemost. 2022;6(4):e12739.
- Revel-Vilk S, Chan A, Bauman M, Massicotte P. Prothrombotic conditions in an unselected cohort of children with venous thromboembolic disease. J Thromb Haemost. 2003;1(5):915-921.
- van Ommen CH, Heijboer H, van den Dool EJ, Hutten BA, Peters M. Pediatric venous thromboembolic disease in one single center: congenital prothrombotic disorders and the clinical outcome. J Thromb Haemost. 2003;1(12):2516-2522.
- Klaassen IL, van Ommen CH, Middeldorp S. Manifestations and clinical impact of pediatric inherited thrombophilia. Blood. 2015;125(7):1073-1077.
- Holzhauer S, Goldenberg NA, Junker R, Heller C, Stoll M, Manner D, et al. Inherited thrombophilia in children with venous thromboembolism and the familial risk of thromboembolism: an observational study. Blood. 2012;120(7):1510-1515.
- Nowak-Gottl U, Kurnik K, Manner D, Kenet G. Thrombophilia testing in neonates and infants with thrombosis. Semin Fetal Neonatal Med. 2011;16(6):345-348.
- Kenet G, Aronis S, Berkun Y, Bonduel M, Chan A, Goldenberg NA, et al. Impact of persistent antiphospholipid antibodies on risk of incident symptomatic thromboembolism in children: a systematic review and meta-analysis. Semin Thromb Hemost. 2011;37(7):802-809.
- Kenet G, Lutkhoff LK, Albisetti M, Bernard T, Bonduel M, Brandao L, et al. Impact of thrombophilia on risk of arterial ischemic stroke or cerebral sinovenous thrombosis in neonates and children: a systematic review and meta-analysis of observational studies. Circulation. 2010;121(16):1838-1847.
- Young G, Albisetti M, Bonduel M, Brandao L, Chan A, Friedrichs F, et al. Impact of inherited thrombophilia on venous thromboembolism in children: a systematic review and meta-analysis of observational studies. Circulation. 2008;118(13):1373-1382.
- Middeldorp S, Nieuwlaat R, Baumann Kreuziger L, Coppens M, Houghton D, James AH, et al. American Society of Hematology 2023 guidelines for management of venous thromboembolism: thrombophilia testing. Blood Adv. 2023;7(22):7101-7138.
- Maher K, Persa L, Barry D, Lee-Eng J, Dichek H, Joshi S, et al. Thrombophilia screening in the routine clinical care of children with arterial ischemic stroke. Pediatr Blood Cancer. 2023;70(8):e30381.
- Kumar R, Sun LR, Rodriguez V, Sankar A, Sharma M, Meoded A, et al. Hemostatic and Thrombotic Considerations in the Diagnosis and Management of Childhood Arterial Ischemic Stroke: A Narrative Review. Semin Pediatr Neurol. 2022;43:101003.
- Saliba E, Debillon T, Recommandations accident vasculaire cerebral n, Auvin S, Baud O, Biran V, et al. [Neonatal arterial ischemic stroke: Review of the current guidelines]. Arch Pediatr. 2017;24(2):180-188.
- Stevens SM, Woller SC, Bauer KA, Kasthuri R, Cushman M, Streiff M, et al. Guidance for the evaluation and treatment of hereditary and acquired thrombophilia. J Thromb Thrombolysis. 2016;41(1):154-164.
- Thornburg CD, Dixon N, Paulyson-Nunez K, Ortel T. Thrombophilia screening in asymptomatic children. Thromb Res. 2008;121(5):597-604.
- Whitworth H, Clark HH, Hubbard RA, Witmer C, Leonard CE, Raffini L. High rate of recurrent venous thromboembolism in children and adolescents with unprovoked venous thromboembolism. J Thromb Haemost. 2023;21(1):47-56.
- Minford A, Brandao LR, Othman M, Male C, Abdul-Kadir R, Monagle P, et al. Diagnosis and management of severe congenital protein C deficiency (SCPCD): Communication from the SSC of the ISTH. J Thromb Haemost. 2022;20(7):1735-1743.
- Price VE, Ledingham DL, Krumpel A, Chan AK. Diagnosis and management of neonatal purpura fulminans. Semin Fetal Neonatal Med. 2011;16(6):318-322.
- O’Brien SH, Badawy SM, Rotz SJ, Shah MD, Makarski J, Bercovitz RS, et al. The ASH-ASPHO Choosing Wisely Campaign: 5 hematologic tests and treatments to question. Blood Adv. 2022;6(2):679-685.
- Neshat-Vahid S, Pierce R, Hersey D, Raffini LJ, Faustino EV. Association of thrombophilia and catheter-associated thrombosis in children: a systematic review and meta-analysis. J Thromb Haemost. 2016;14(9):1749-1758.
- Powers WJ, Rabinstein AA, Ackerson T, Adeoye OM, Bambakidis NC, Becker K, et al. Guidelines for the Early Management of Patients With Acute Ischemic Stroke: 2019 Update to the 2018 Guidelines for the Early Management of Acute Ischemic Stroke: A Guideline for Healthcare Professionals From the American Heart Association/American Stroke Association. Stroke. 2019;50(12):e344-e418.
- Curtis C, Mineyko A, Massicotte P, Leaker M, Jiang XY, Floer A, et al. Thrombophilia risk is not increased in children after perinatal stroke. Blood. 2017;129(20):2793-2800.
Informations complémentaires
Auteur·e·s
-
PD Dr med. et phil. Mattia RizziMédecin Associé, Unité d’Hématologie-Oncologie, Service de Pédiatrie, Hôpital des Enfants, CHUV, Lausanne
