Bilan d’hémostase chez l’enfant : quand y penser ? Indications, particularités et challenges
Introduction
L’hémostase pédiatrique est un système dynamique et en développement évoluant progressivement de la vie fœtale jusqu’à l’âge adulte(1).
Le concept de l’hémostase en développement remonte à la fin des années 80, quand la Dr. Andrew avait montré, avec ses publications sur une grande cohorte de nouveau-nés et de nourrissons, que les taux fonctionnels de la majorité des protéines de la coagulation varient avec l’âge(1,2). Toutefois, la compréhension des mécanismes et des implications liées à ces changements s’avère, encore de nos jours, limitée(2). Nombreux auteurs ont essayé d’actualiser les normes et les valeurs de référence des différents facteurs de coagulation chez l’enfant à l’aide de réactifs récents, mais les difficultés dans le recrutement de jeunes enfants en bonne santé, en ont limité les résultats(3,4). Toutefois, bien que les valeurs absolues des différentes protéines de la coagulation dépendent des réactifs et du type d’appareil, les tendances s’avèrent cohérentes dans les différentes publications dans le domaine(2).
Les modifications des taux de protéines de la coagulation en fonction de l’âge sont résumées dans le Tableau 1.
Sur le plan physiologique, ces anomalies conduisent chez le nouveau-né et le nourrisson à une :
- Diminution de la génération de thrombine, en lien avec une activité diminuée de la majorité des facteurs procoagulants jusqu’à l’âge de 6 mois, voire plus selon les facteurs
- Diminution de l’activité anticoagulante(5,6)
- Diminution de la fibrinolyse (une augmentation de la fibrinolyse a été toutefois décrite à la naissance)(7,8)
Une hyporéactivité plaquettaire est également décrite en âge néonatal, compensée par une augmentation de l’adhésion ainsi qu’une augmentation de l’activité du facteur de von Willebrand (FVW)(9).
Malgré ces particularités physiologiques, les nouveau-nés et nourrissons en bonne santé ne présentent pas de tendance accrue aux complications hémorragiques ou thrombotiques, ce qui indique un système fonctionnel et en équilibre depuis la naissance (5). Connaître ces modifications, est toutefois essentiel afin d’interpréter correctement les résultats d’un bilan d’hémostase chez l’enfant, en particulier chez le nouveau-né et le nourrisson.
Dans cette revue, nous présenterons tout d’abord trois situations cliniques dans lesquelles la réalisation d’un bilan d’hémostase peut être indiquée chez l’enfant, puis nous résumerons l’approche biologique appropriée.
Indication à un bilan d’hémostase en âge pédiatrique
1. Bilan préopératoire
Un bilan préopératoire de routine n’est, de nos jours, plus recommandé par la majorité des sociétés savantes d’anesthésie. La plupart des lignes directrices et des avis d’expert·e·s déconseillent la réalisation systématique d’examens préopératoires de l’hémostase et recommandent plutôt de personnaliser les examens en fonction du contexte clinique(10). Font exception les jeunes enfants qui n’ont pas encore acquis la marche, chez lesquels la société française d’anesthésie préconise d’effectuer un dosage du temps de thromboplastine partielle activé (aPTT) et une numération plaquettaire avec toutefois un degré d’évidence faible(11).
Ces recommandations sont supportées par de nombreuses publications qui montrent l’absence de corrélation entre les résultats du screening préopératoire et le taux de complications hémorragiques intra- ou post-opératoire(11,12). En effet, un bilan de dépistage permet d’identifier seulement un petit nombre d’enfants avec risque hémorragique avant chirurgie(13).
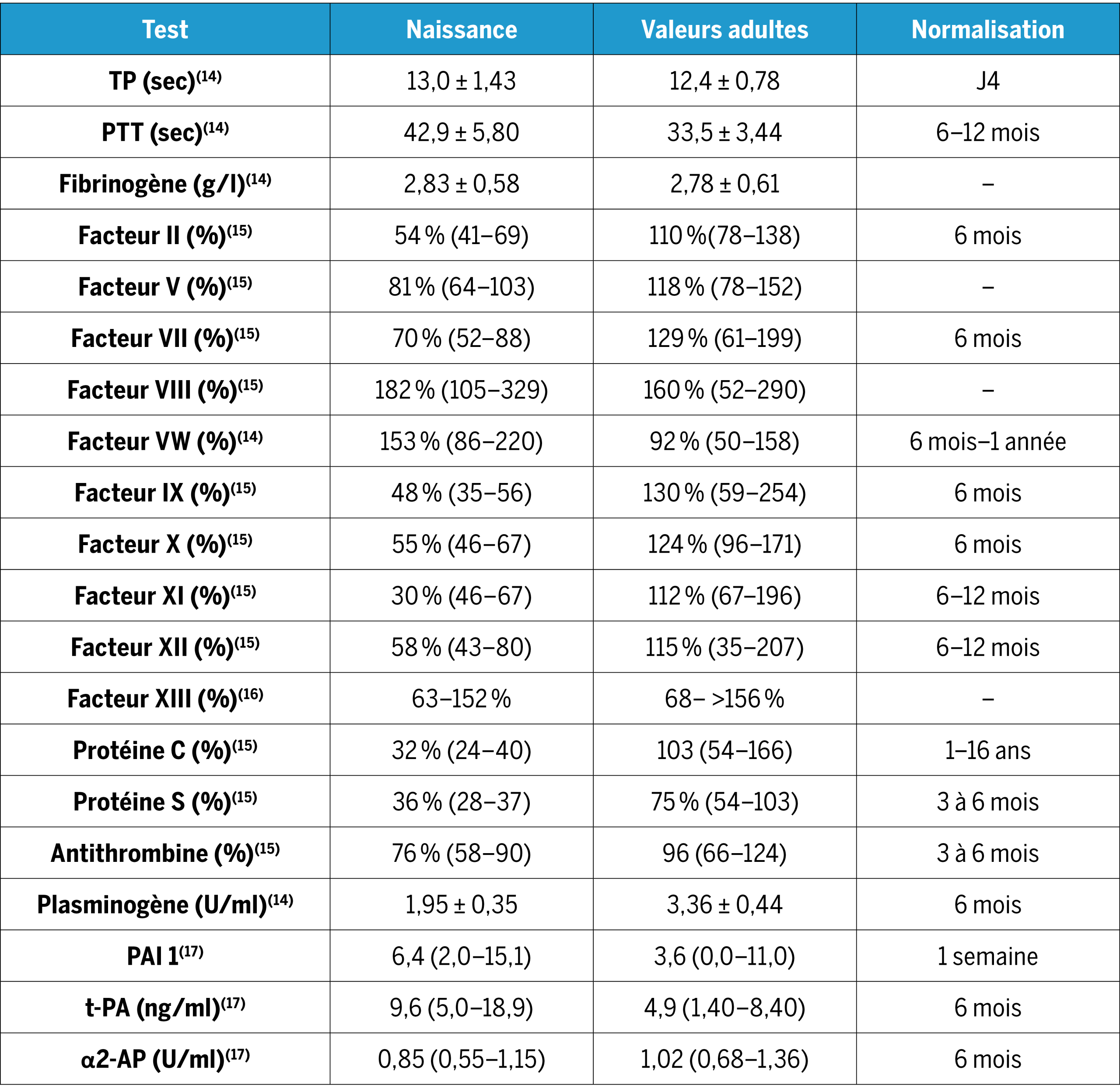
Adapté de Andrew et al. (1987)(14), Monagle et al. (2006)(15), Appel et al. (2012)(16), Parmar et al. (2006)17) FVW : Facteur de von Willebrand, TP : temps de prothrombine, PTT : temps de thromboplastine partielle activé, PAI : inhibiteur de l’activateur du plasminogène, t-PA : activateur tissulaire du plasminogène, α2-AP : α2-antiplasmine
Ceci est particulièrement lié à la faible prévalence de coagulopathies héréditaires ainsi qu’un nombre élevé de faux positifs (p. exemple allongement du PTT en présence d’anticoagulant lupique (cf. figure 2)(18).
Les expert·e·s recommandent plutôt en préopératoire une anamnèse structurée, en limitant les investigations aux patients avec un phénotype hémorragique, quel que soit le type de chirurgie(19). Chez l’enfant, il faut également considérer l’importance d’une anamnèse familiale positive, comme le stipule le paragraphe suivant.
Afin de mieux évaluer le risque hémorragique peropératoire des questionnaires standardisés sont régulièrement utilisés chez l’adulte pour identifier les patients présentant des troubles de la coagulation(11). Une étude prospective pédiatrique récente a montré une bonne prédiction du risque hémorragique avant chirurgie d’adénoïdectomie et amygdalectomie également chez l’enfant à l’aide d’un questionnaire standardisé adapté(20).
2. Diathèse hémorragique
Le défi pour les pédiatres qui évaluent un enfant présentant un trouble hémorragique potentiel est de déterminer si les symptômes sont liés à un trouble de la coagulation (congénital ou acquis) ou si au contraire, il s’agit de symptômes banaux qui peuvent se produire couramment chez les enfants en bonne santé et qui ne nécessitent donc pas d’investigations(21). Ceci est primordial afin de prendre en charge de façon appropriée les symptômes et de minimiser le risque hémorragique en cas d’interventions chirurgicales.
Une anamnèse ciblée personnelle et familiale s’avère donc fondamentale dans l’approche diagnostique.
Avant toute investigation, il est important d’exclure à l’anamnèse toute prise de médicaments susceptibles d’interférer avec l’hémostase, notamment les anti-inflammatoires (anti-COX1), les anticoagulants, les antidépresseurs (SSRI), ainsi que certains produits phytothérapeutiques (gingembre, Ginko biloba, etc…)(1). Des conditions cliniques telles qu’une pathologie hépatique, rénale ou thyroïdienne doivent également être recherchées, dans la mesure où elles peuvent s’associer à une tendance hémorragique acquise(22).
La possibilité d’un trouble de la coagulation sous-jacent doit être envisagée chez les enfants qui présentent des symptômes hémorragiques qui sont : anormalement fréquents, de longue durée et sévères(1).
Plusieurs éléments anamnestiques vont contribuer à préciser le diagnostic :
La localisation des symptômes : les troubles de l’hémostase primaire (tels que la maladie de von Willebrand et les troubles de la fonction plaquettaire) se manifestent principalement par des saignements muqueux (saignements utérins anormaux, épistaxis, purpura), alors que les troubles de l’hémostase secondaires (tels que l’hémophilie, ou d’autres déficits en facteurs de coagulation) ont tendance à se manifester plutôt par des saignements articulaires, musculaires ou profonds(23). Un saignement persistant du cordon ombilical ou une hémorragie intracrânienne (HIC) néonatale peuvent se manifester dans le cadre d’une afibrinogénémie ou un déficit sévère en FXIII(9). Des déficits sévères en FX sont aussi associés à des HICs néonatales(24).
Il est également important de rappeler que 20 à 30% des adolescentes présentant des saignements utérins anormaux pourraient avoir un trouble de l’hémostase sous-jacente. Dans cette catégorie de patientes, il est donc tout particulièrement important de rechercher une tendance hémorragique et d’exclure d’autres causes de ménorragie avec une approche multidisciplinaire(25).
L’âge de début des symptômes : plus précoce est l’apparition des symptômes, plus il est probable qu’il s’agisse d’un déficit congénital (notamment sévère). Un âge plus tardif oriente vers un trouble modéré de l’hémostase ou une pathologie acquise(26). Des symptômes néonataux tels qu’un céphalhématome, une hémorragie ombilicale à la chute du cordon ou un hématome de succion doivent systématiquement être recherchés et peuvent suggérer une maladie hémorragique congénitale(1).
La sévérité des saignements : la présence d’une carence en fer ou d’une anémie associée et la nécessité éventuelle d’un traitement complémentaire (acide tranexamique, desmopressine, transfusion) font également suspecter un trouble de la coagulation sous-jacent.
Le mode d’apparition : un saignement spontané suggère une pathologie sévère(23). Une apparition aiguë sur une période allant de quelques jours à quelques semaines suggère une maladie acquise (comme une carence en vitamine K, par exemple) alors que des symptômes persistants depuis longtemps indiquent une maladie hémorragique congénitale potentielle (21).
L’anamnèse familiale est particulièrement importante en pédiatrie, car la plupart des enfants n’ont pas eu de challenges hémostatiques (intervention chirurgicale, traumatisme), ce qui rend le diagnostic difficile, notamment concernant les syndromes hémorragiques dits « mineurs » (maladie de von Willebrand, thrombopathie mineure). L’anamnèse familiale doit inclure des questions sur les interventions chirurgicales antérieures, les extractions dentaires et les transfusions de tous les membres de la famille, ainsi que sur les antécédents menstruels et obstétricaux des femmes de la famille(21). Une anamnèse familiale négative n’exclut en revanche pas un trouble de la coagulation. Notamment environ 30 % des enfants diagnostiqués avec une hémophilie n’ont pas d’antécédents familiaux (mutation de novo)(27).
Des questionnaires d’évaluation des saignements ou « bleeding assessement tools (BAT) », ont été développés afin de mesurer de manière plus précise les symptômes hémorragiques chez les patients. Ces questionnaires, développés initialement pour le diagnostic de la maladie de von Willebrand, présentent une sensibilité élevée dans le dépistage des certains troubles héréditaires de l’hémostase(28). Le plus utilisé est le BAT de la Société internationale de thrombose et d’hémostase (ISTH). Avec ce questionnaire, les manifestations hémorragiques sont évaluées en fonction de leur gravité avec une échelle de 1 à 4. Un score ≥ 3 s’avère pathologique chez l’enfant suggérant un trouble de la coagulation(29). Les critères pour définir une diathèse hémorragique comme significative selon l’ISTH-BAT sont repris dans le Tableau 2(30).
L’examen clinique : une maladie hémorragique congénitale ou acquise doit être recherchée en présence de :
- Signes hémorragiques cutanés (ecchymoses, pétéchies, hématomes, télangiectasies) ou muqueuses (gencives, bulles hémorragiques)
- Déformations articulaires ou limitation des amplitudes articulaires parlant en faveur d’une arthropathie
- Hépatosplénomégalie ou présence d’adénopathies associées à un purpura ou une diathèse hémorragique évoquant une maladie oncologique sous-jacente(23).
- Signes dysmorphiques pouvant être présents dans le cadre d’une thrombopénie ou thrombopathie congénitale.
3. Suspicion de maltraitance
Face à une suspicion de maltraitance, les pédiatres sont amenés à se prononcer sur l’origine de manifestations clinique telles que des ecchymoses ou des saignements inhabituels, notamment intracérébraux, mais aussi des saignements gastro-intestinaux, des hémorragies rétiniennes, des hémorragies intraspinales et des hémarthroses(31).
Dans ce contexte, un bilan d’hémostase s’avère essentiel afin d’exclure une diathèse hémorragique sous-jacente. Une rare exception est la présence de blessures multiples (cutanés, osseuses…) clairement compatibles avec une anamnèse de traumatismes non accidentels répétés et cohérents avec l’histoire clinique.
En effet, les ecchymoses attribuables à des traumatismes accidentels courants chez les enfants ont tendance à être relativement petites, de forme ovale ou arrondie, mais sans bordure distincte, situées au-dessus ou près de proéminences osseuses à l’avant du corps (souvent le front, les genoux ou les tibias). Les ecchymoses touchant les oreilles, le cou, les joues, les yeux et les parties génitales restent rares et s’avèrent donc suspectes de maltraitance, ainsi que des ecchymoses linéaires ou avec un tracé reconnaissable (p. ex., l’empreinte d’une main ou d’une semelle)(32). Les ecchymoses chez les enfants non encore mobiles sont également plus susceptibles d’être secondaires à une maltraitance physique.
Les HICs peuvent être dues à un effet de force directe résultant de coups avec impact sur le crâne ou à un effet de force indirecte (secousses) généralement appelé « syndrome du bébé secoué ». Dans ce second cas, on observe également des hémorragies rétiniennes, pathognomoniques de maltraitance dans le contexte(33).
Une carence en vitamine K doit également être évoqué chez les nourrissons âgés de 0 à 3 mois qui présentent ecchymoses et des hémorragies gastro-intestinales ou intracrâniennes importantes(31).
Il est toutefois important de souligner qu’un diagnostic de maltraitance n’exclut pas une diathèse hémorragique associée et, inversement, qu’un diagnostic de diathèse hémorragique congénitale ou acquise ne permets pas d’écarter formellement une maltraitance, surtout en présence d’une anamnèse suspecte.
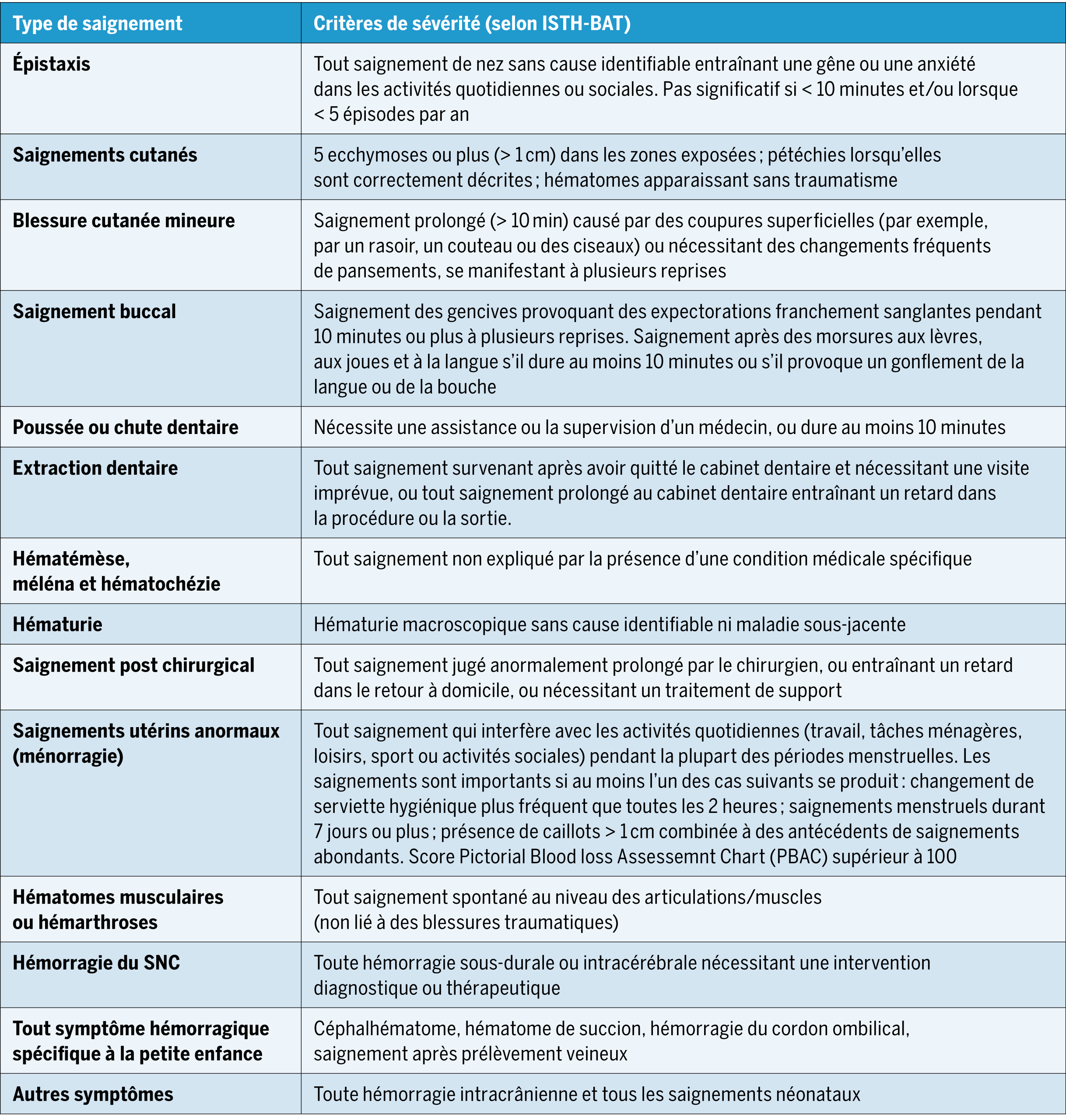
Adapté de Rodeghiero et al. (2019)(30) ISTH-BAT : Société Internationale de thrombose et hémostase-Bleeding assessment tool
En conclusions, face à une suspicion de maltraitance, un bilan de diathèse hémorragique doit être envisagé en présence de :
- ecchymoses chez un enfant non mobile.
- ecchymoses inhabituelles et/ou saignements disproportionnés par rapport au mécanisme présumé.
- saignement à un endroit critique (par exemple, hémorragie intracérébrale, hémorragie rétinienne, hémorragie gastro-intestinale, hémorragie intraspinale, hémarthrose) sans antécédents correspondants de traumatisme ou autre explication qui justifie de manière adéquate le saignement.
- suspicion de coagulopathie d’après les antécédents personnels, les antécédents familiaux et/ou l’examen(31).
Quel bilan effectuer ?
1. Bilan de diathèse hémorragique
Face à une diathèse hémorragique, une approche en plusieurs étapes est généralement utilisée avec quelque différences mineures selon les centres(22).
1.1. Bilan initial (cf. Figure 1)
Les expert·e·s recommandent en première intention :
- Une formule sanguine avec numération plaquettaire.
Cette analyse permet de mettre en évidence une thrombocytopénie ainsi que des anomalies du volume plaquettaire (suggérant possiblement une pathologie plaquettaire sous-jacente)(34). La présence d’une anémie associée à une diathèse hémorragique peut, en outre, suggérer des saignements plus sévères et de longue durée. Dans la pratique courante, un dosage de la ferritinémie est également suggéré afin de déceler un état ferriprive associé, indice d’une spoliation dans le cadre de saignements répétés(21). De plus , le frottis sanguin permet d’obtenir des informations supplémentaires sur la taille et la granularité des plaquettes et d’analyser l’aspect des autres cellules sanguines (inclusions intracytoplasmiques, présence de cellules pathologiques)(23,26). - Un dosage du temps de prothrombine (TP), du PTT et du fibrinogène.
En cas de score ISTH-BAT pathologique, le dosage des activités des facteurs IX, et XI est souvent recommandé en première intention, car les déficits légers peuvent échapper au PTT(22). Un dosage du FXIII est également recommandé en première intention, un déficit n’ayant pas d’impact sur les temps de coagulation. - Un dosage de l’activité fonctionnelle du facteur de von Willebrand (FVW)
Bien que le test FVW:RCo (activité cofacteur de la ristocétine) soit le test traditionnellement utilisé pour mesurer l’activité du FVW, des tests plus récents tels que le FVW:GPIbM (activité de liaison aux plaquettes) sont généralement plus reproductibles et sont de plus en plus utilisés. Un dosage de l’activité du facteur VIII est en général effectué en même temps(21,35). La connaissance du groupe sanguin est importante pour l’interprétation des résultats. La concentration plasmatique en FVW est significativement influencée par le groupe sanguin ABO. En fait, le groupe sanguin O est associé aux valeurs les plus faibles de FVW sans évidence de modifications structurelles ou moléculaires(36,37). - Une analyse de la fonction plaquettaire par agrégométrie par transmission de lumière (LTA).
Le LTA est le test de référence pour analyser la fonction plaquettaire. Elle mesure la réponse plaquettaire (agrégation) à un panel d’agonistes (collagène, ADP, ristocétine, adrénaline, acide arachidonique, TRAP, U46619)(38). Ce test nécessite une expertise médicale pour l’interprétation des résultats et est effectué dans des laboratoires spécialisés. Il faut toutefois mentionner que cette analyse peut s’avérer difficile chez le petit enfant en raison du volume important de sang nécessaire. En cas de résultats pathologiques, selon le profil d’agrégation, des analyses complémentaires peuvent s’avérer nécessaires afin de préciser le type de dysfonction plaquettaire (analyse de la sécrétion plaquettaire, des protéines membranaires par cytométrie en flux, microscopie électronique afin d’analyser le contenu granulaire, complétés par des analyses génétiques ciblés ou à large spectre)(38).
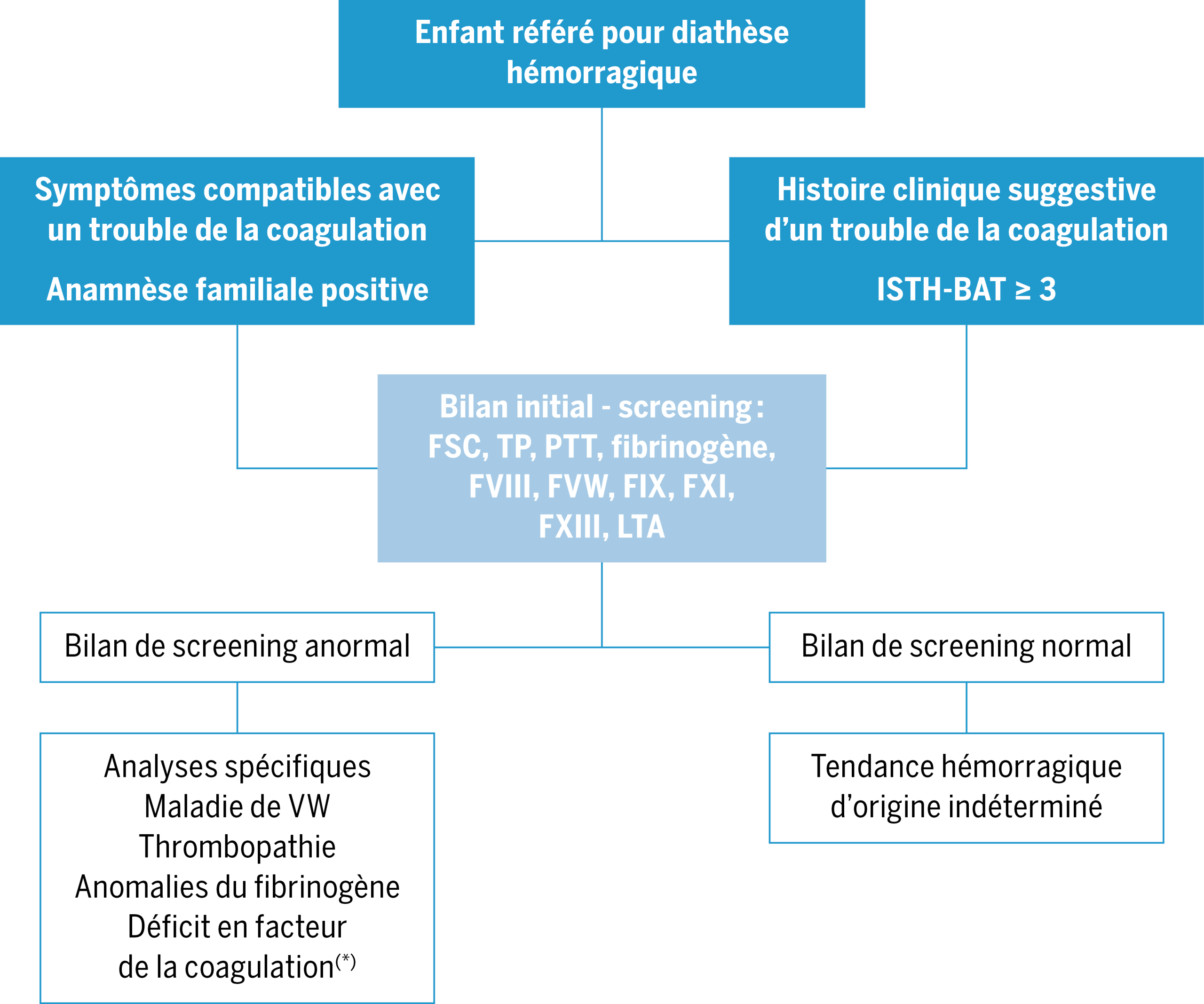
Adapté de Casini, Alessandro et Johanna Gebhart. « How to Investigate Mild to Moderate Bleeding Disorders and Bleeding Disorder of Unknown Cause ». International Journal of Laboratory Hematology 46 Suppl 1 (mai 2024): 27‑33. https://doi.org/10.1111/ijlh.14266. ISTH-BAT : Société Internationale de thrombose et hémostase – Bleeding assessement tool; TP : temps de prothrombine; PTT : temps de thromboplastine partielle activée; VW: Von Willebrand; LTA : agrégométrie par transmission de lumière
(*) Pour le détail des analyses complémentaires en cas d’allongement du PTT et/ou du TP cf. figures 2 & 3.
1.2. Bilan complémentaire en présence d’anomalies lors du bilan de screening (cf. Figure 1)
- Selon le résultat du bilan initial, des investigations complémentaires s’avèrent nécessaires à la recherche d’un déficit factoriel en cas d’anomalies du du PTT et/ou du TP (cf. Figure 2 & 3). En cas d’hémophilie A légère ou modérée un dosage du FVIII chromogénique est également recommandé. En cas de résultats suggérant un trouble du fibrinogène, un dosage du taux de fibrinogène (antigène) ainsi que des temps de thrombine et reptilase est recommandé pour aider à distinguer entre les désordres quantitatifs (hypo ou afibrinogénémie) et qualitatifs ((hypo)-dysfibrinogénémie) (39). Ces analyses seront à compléter par des investigations génétiques et sont du ressort d’un centre spécialisé dans les anomalies du fibrinogène.
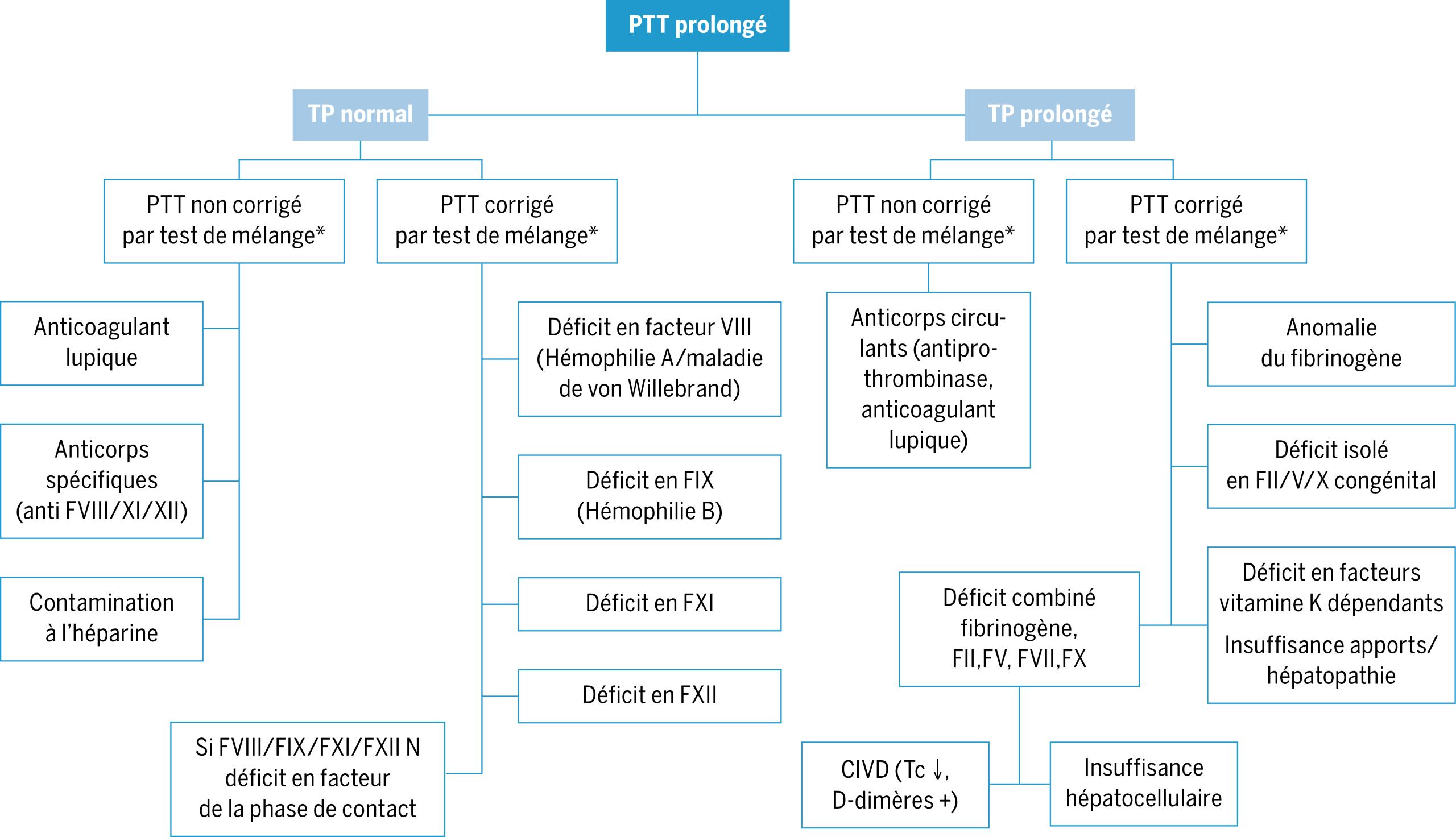
Adapté de Chambost, H. « Démarche diagnostique devant un allongement du TCA ». Archives de Pédiatrie 18, no 5 (2011): H38‑39. https://doi.org/10.1016/S0929-693X(11)71088-0. PTT : temps de thromboplastine partielle activée; TP : temps de prothrombine, CIVD: coagulation intravasculaire disséminée, Tc: thrombocytes (*) Le Test de mélange est effectué en mélangeant le plasma du patient avec le plasma d’un témoin sans anomalie de la coagulation.
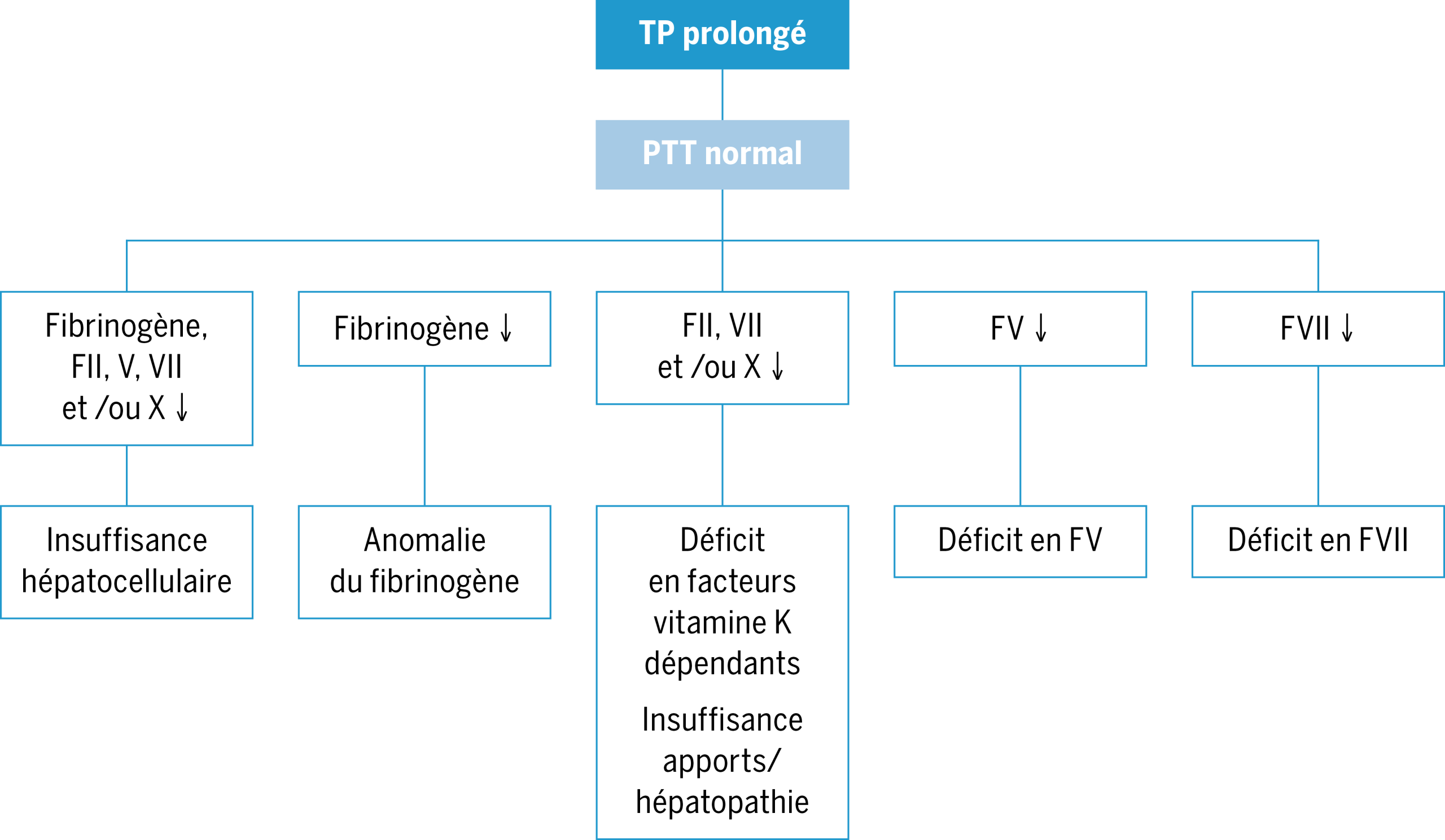
Adapté de Société française d’hématologie. Guide des analyses en hématologie. 1ère éd. Elsevier Masson, 2018. https://www.elsevier.com/fr-fr/connect/guide-des-analyses-en-hematologie. TP : temps de prothrombine, PTT: temps de thromboplastine partielle activée.
- En cas de suspicion de maladie de von Willebrand des analyses complémentaires (telles que le dosage antigénique, la mesure du taux de liaison au collagène et du taux de liaison au FVIII, l’électrophorèse des multimères du FVW, l’agrégation à la ristocétine, ainsi qu’éventuellement des tests génétiques) sont nécessaires afin de préciser le type de maladie de von Willebrand(35). Ces tests nécessitent d’un laboratoire spécialisé et de compétences spécifiques pour l’interprétation des résultats.
La présence d’anomalie de la fibrinolyse peut être envisagée dans un deuxième temps lorsque les examens préliminaires sont normaux et que le type d’hémorragie (par exemple, hémorragie intracrânienne, hémorragie tardive après chirurgie) justifie des examens complémentaires(38). Cependant, à l’heure actuelle, on ne dispose pas de tests diagnostiques fiables pour diagnostiquer ou dépister les troubles fibrinolytiques, de ce fait, leur utilisation clinique n’est pas recommandée(22).
Il convient de souligner que la majorité des patients présentant une tendance hémorragique significative ont un bilan de diathèse hémorragique normal. Ces patients, classés dans le groupe des tendances hémorragiques d’origine indéterminée, nécessitent néanmoins une prise en charge comparable à celle des patients présentant une anomalie de l’hémostase confirmée(22).
Des tests globaux de la coagulation sont de plus en plus utilisés, notamment au sein de centres hospitaliers et universitaires. Il s’agit de :
- la thromboélastographie (TEG ou ROTEM) : test qui évalue la formation du caillot et sa stabilité sur sang total, généralement utilisé dans la gestion per- et post-opératoire.
- le test de génération de thrombine (TG) qui évalue l’activation, la propagation et l’inhibition de la coagulation. Les limites de ce test sont dues à un manque de standardisation et à d’importantes variations quantitatives dans les résultats.
L’utilité clinique de ces tests reste à déterminer, ainsi ces tests ne sont actuellement pas recommandés dans le cadre d’un dépistage d’une diathèse hémorragique(30).
En cas de suspicion de maltraitance, en plus du bilan de diathèse hémorragique susmentionné un dosage des D-dimères est également recommandé en cas de compromission neurologique afin d’exclure une coagulopathie intravasculaire disséminée(40).
Challenges
Le dépistage des complications hémorragiques ou thrombotiques chez les nouveau-nés et les enfants présente de nombreux pièges et difficultés supplémentaires par rapport à un bilan effectué chez un adulte(2).
En premier lieu, il faut mentionner l’importance des variables pré-analytiques :
- L’obtention d’une quantité suffisante de sang par ponction veineuse peut s’avérer extrêmement difficile chez les nourrissons, ce qui conduit à une activation de la coagulation dans l’échantillon. Par ailleurs, les tubes de prélèvement sont souvent insuffisamment remplis, ce qui empêche d’atteindre le rapport citrate/sang nécessaire à l’analyse, conduisant à des non-conformités, des retards diagnostiques et souvent des ponctions répétées(2,4).
- Les échantillons sanguins sont fréquemment prélevés via des cathéters périphériques ou centraux, ce qui entraîne une activation de l’échantillon ou une contamination par l’héparine, qui perturbent les résultats d’analyse(4).
- Chez le nouveau-né, on observe une polyglobulie relative, physiologique, qui nécessite toutefois un ajustement du volume de citrate dans le tube d’analyse. Dans la même population, la présence d’hyperbilirubinémie, dans le cadre d’un ictère physiologique, peut également interférer avec les automates qui utilisent une méthode optique pour la détection du caillot(2).
En deuxième lieu, comme mentionné dans l’introduction, l’hémostase en âge pédiatrique est un système en développement. La plupart des résultats des tests de coagulation chez l’enfant doivent donc être interprétés selon des normes adaptées à l’âge afin d’en garantir un diagnostic précis et correct(41). En 2012, l’ISTH a publié des recommandations destinées aux enfants, précisant que les laboratoires d’hémostase devraient utiliser des intervalles de référence spécifiques à la population, aux réactifs et aux appareils(3). Ces directives sont toutefois contraignantes et parfois difficiles à réaliser (population restreinte, coûts élevés). Une alternative acceptable, comme suggéré par Toulon dans une revue sur l’hémostase en développement, serait de traduire les conclusions de la littérature en plages de référence locales pour les nouveau-nés et les enfants, en tenant compte des données disponibles pour les combinaisons de réactifs et automates le plus fréquemment utilisés(7).
Lors de l’interprétation d’un bilan de diathèse hémorragique il faut également considérer que les taux de facteur VIII, du FVW et du fibrinogène peuvent être augmentés par l’exercice, le stress, une infection , une tumeur maligne ou une intervention chirurgicale récente(22). On observe également des variations du taux d’activité du FVW au cours du cycle menstruel et en association avec un traitement hormonal(30). Parfois des dosages répétés des facteurs de coagulation sont donc nécessaires afin d’ établir un diagnostic précis(22).
Conclusions
La réalisation d’un bilan de coagulation chez l’enfant doit être justifié par le contexte clinique et les antécédents familiaux.
Une bonne interprétation du bilan d’hémostase chez l’enfant nécessite en amont une bonne évaluation sémiologique des manifestations cliniques (contexte, fréquence, localisation, facteurs de risque, comorbidités). Elle doit également tenir compte de l’âge de l’enfant ainsi que des comorbidités pouvant altérer les résultats (p. exemple état inflammatoire). Des bilans répétés sont souvent nécessaires afin de confirmer un diagnostic.
En cas de suspicion d’une anomalie de l’hémostase, une consultation spécialisée par un médecin expert en hémostase est recommandée afin de confirmer le diagnostic et planifier une prise en charge adéquate.
Références
- Meunier S. Comment explorer un syndrome hémorragique de l’enfant? Perfectionnement en Pédiatrie. 2020;3(3):250‑9.
- Monagle P, Ignjatovic V, Savoia H. Hemostasis in neonates and children: Pitfalls and dilemmas. Blood Reviews. mars 2010;24(2):63‑8.
- Ignjatovic V, Kenet G, Monagle P. Developmental hemostasis: recommendations for laboratories reporting pediatric samples. Journal of Thrombosis and Haemostasis. févr 2012;10(2):298‑300.
- Rahman M, George C, Monagle P. Hot topics in coagulation testing: Important considerations for testing children for bleeding/thrombotic disorders. Int J Lab Hematology. juin 2020;42(S1):68‑74.
- Pal S, Curley A, Stanworth SJ. Interpretation of clotting tests in the neonate: Table 1. Arch Dis Child Fetal Neonatal Ed. mai 2015;100(3):F270‑4.
- Lippi G, Franchini M, Montagnana M, Guidi G. Coagulation Testing in Pediatric Patients: The Young Are Not Just Miniature Adults. Semin Thromb Hemost. nov 2007;33(8):816‑20.
- Toulon P. Developmental hemostasis: laboratory and clinical implications. Int J Lab Hematology. mai 2016;38(S1):66‑77.
- Albisetti M. The Fibrinolytic System in Children.
- Kenet G, Nowak-Göttl U. Bleeding and Thrombosis Issues in Pediatric Patients: Current Approach to Diagnosis and Treatment. Acta Haematol. 2006;115(3‑4):137‑40.
- Jover Pinillos JL, Ferrandis Comes R, Zamudio Penko D, Bermúdez López M, Basora Macaya M, Colomina Soler MJ. Preoperative coagulation tests: A narrative review of current guidelines. Revista Española de Anestesiología y Reanimación (English Edition). déc 2024;71(10):740‑7.
- Bonhomme F, Ajzenberg N, Schved JF, Molliex S, Samama CM. Pre-interventional haemostatic assessment: Guidelines from the French Society of Anaesthesia and Intensive Care. European Journal of Anaesthesiology. avr 2013;30(4):142‑62.
- Krishna P, Lee D. Post‐Tonsillectomy Bleeding: A Meta‐Analysis. The Laryngoscope. août 2001;111(8):1358‑61.
- Gabriel P, Mazoit X, Ecoffey C. Relationship Between Clinical History, Coagulation Tests, and Perioperative Bleeding During Tonsillectomies in Pediatrics. Journal of Clinical Anesthesia. 2000;(12):288‑91.
- Andrew M, Paes B, Milner R, Johnston M, Mitchell L, Tollefsen D, et al. Development of the human coagulation system in the full-term infant. Blood. 1 juill 1987;70(1):165‑72.
- Monagle P, Barnes C, Ignjatovic V, Furmedge J, Newall F, Chan A, et al. Developmental haemostasis: Impact for clinical haemostasis laboratories. Thromb Haemost. 2006;95(02):362‑72.
- Appel IM, Grimminck B, Geerts J, Stigter R, Cnossen MH, Beishuizen A. Age dependency of coagulation parameters during childhood and puberty. Journal of Thrombosis and Haemostasis. nov 2012;10(11):2254‑63.
- Parmar N, Albisetti M, Berry LR, Chan AKC. The fibrinolytic system in newborns and children. Clin Lab. 2006;52(3‑4):115‑24.
- Burk CD, Miller L, Handler SD, Cohen AR. Preoperative history and coagulation screening in children undergoing tonsillectomy. Pediatrics. avr 1992;89(4 Pt 2):691‑5.
- Zamudio Penko D, Cancho García D, Bartolomé Ruibal A, Gijón Herreros N, Redondo Martínez P, Gisbert de la Cuadra L, et al. Preoperative coagulation screening tests in pediatric patients: Clinical relevance and hemorrhagic outcomes of abnormal results. Revista Española de Anestesiología y Reanimación (English Edition). févr 2023;70(2):68‑76.
- Masalha M, DeRowe A, Mazzawi S, Chen T, Ghanayim R, Landsberg R, et al. Coagulation tests or standardized questionnaire, which is better as a predictor of bleeding? A prospective study among children before tonsillectomy and/or adenoidectomy. BMC Res Notes. déc 2020;13(1):175.
- Allen GA, Glader B. Approach to the bleeding child. Pediatr Clin North Am. déc 2002;49(6):1239‑56.
- Casini A, Gebhart J. How to investigate mild to moderate bleeding disorders and bleeding disorder of unknown cause. Int J Lab Hematol. mai 2024;46 Suppl 1:27‑33.
- Harroche A, Rothschild C. Diagnostic d’un syndrome hémorragique de l’enfant. Journal de Pédiatrie et de Puériculture. 2019;32(1):1‑11.
- Brown DL, Kouides PA. Diagnosis and treatment of inherited factor X deficiency. Haemophilia. nov 2008;14(6):1176‑82.
- Casini A, Moussaoui D, Crofts VL, Mattiello V, Yaron M, Fontana P. Saignements utérins anormaux et anomalies de l’hémostase. Revue Médicale Suisse. 2024;20(898):2271‑5.
- Roberts JC. Evaluation of Abnormal Bleeding in Children. Pediatr Ann. 1 janv 2020;49(1):e36‑42.
- Srivastava A, Santagostino E, Dougall A, Kitchen S, Sutherland M, Pipe SW, et al. WFH Guidelines for the Management of Hemophilia, 3rd edition. Haemophilia. août 2020;26(S6):1‑158.
- Alhuniti A, Abdallah H, Rand ML, Kearney S, Sharathkumar AA, Sridharan M, et al. Accuracy of a Bleeding Assessment Tool in Predicting the Diagnosis of an Inherited Bleeding Disorder: Systematic Review and Meta-Analysis. Blood. 5 nov 2024;144(Supplement 1):1217‑1217.
- Rodeghiero F, Tosetto A, Abshire T, Arnold DM, Coller B, James P, et al. ISTH/SSC bleeding assessment tool: a standardized questionnaire and a proposal for a new bleeding score for inherited bleeding disorders. Journal of Thrombosis and Haemostasis. sept 2010;8(9):2063‑5.
- Rodeghiero F, Pabinger I, Ragni M, Abdul‐Kadir R, Berntorp E, Blanchette V, et al. Fundamentals for a Systematic Approach to Mild and Moderate Inherited Bleeding Disorders: An EHA Consensus Report. HemaSphere. oct 2019;3(5):e286.
- Biss T, Sibson K, Baker P, Macartney C, Grayson C, Grainger J, et al. Haematological evaluation of bruising and bleeding in children undergoing child protection investigation for possible physical maltreatment: A British Society for Haematology Good Practice Paper. Br J Haematol. oct 2022;199(1):45‑53.
- Maguire S, Mann M. Systematic reviews of bruising in relation to child abuse—what have we learnt: an overview of review updates. Evid‐Based Child Health. 7 mars 2013;8(2):255‑63.
- Knöfler R, Streif W, Watzer-Herberth I, Hahn G, Schmidt U. Child Abuse or Bleeding Disorder—An Interdisciplinary Approach. Hamostaseologie. févr 2019;39(01):028‑35.
- Fontana P, Boehlen F. Diagnostic et prise en charge des syndromes hémorragiques dits mineurs. Revue Médicale Suisse.
- James PD, Connell NT, Ameer B, Di Paola J, Eikenboom J, Giraud N, et al. ASH ISTH NHF WFH 2021 guidelines on the diagnosis of von Willebrand disease. Blood Advances. 12 janv 2021;5(1):280‑300.
- Gill JC, Endres-Brooks J, Bauer PJ, Marks WJ, Montgomery RR. The effect of ABO blood group on the diagnosis of von Willebrand disease. Blood. juin 1987;69(6):1691‑5.
- Kienzle D, Munda E, Daskalakis C, Rhoades R. Association of Blood Type with Von Willebrand Disease Severity Among Patients at an Academic Hemophilia Treatment Center. Blood. 5 nov 2024;144(Supplement 1):3983‑3983.
- Hayward CPM. How I investigate for bleeding disorders. Int J Lab Hematol. mai 2018;40 Suppl 1:6‑14.
- Casini A, Undas A, Palla R, Thachil J, De Moerloose P. Diagnosis and classification of congenital fibrinogen disorders: communication from the SSC of the ISTH. Journal of Thrombosis and Haemostasis. sept 2018;16(9):1887‑90.
- Anderst J, Carpenter SL, Abshire TC, Killough E, AAP SECTION ON HEMATOLOGY/ONCOLOGY, THE AMERICAN SOCIETY OF PEDIATRIC HEMATOLOGY/ONCOLOGY, THE AAP COUNCIL ON CHILD ABUSE AND NEGLECT, Consultants, et al. Evaluation for Bleeding Disorders in Suspected Child Abuse. Pediatrics. 1 oct 2022;150(4):e2022059276.
- Toulon PA, Arcizet J, Grand F, De Pooter N, Lasnes D, Brionne-François M. Age Dependency Of Coagulation Parameters During Childhood. Blood. 15 nov 2013;122(21):2341‑2341.
Informations complémentaires
Auteur·e·s
-
Dr. med. Veneranda MattielloUnité d'onco-hématologie pédiatrique, Service de Pédiatrie générale, Département de la Femme de l’Enfant et de l’Adolescent, Hôpitaux Universitaires de Genève
-
Prof. Dr med. Alessandro CasiniUnité d’hémostase, Service d’Angiologie et hémostase, Département de Médecine Interne, Hôpitaux Universitaires de Genève
