Einleitung
Thromboembolische Ereignisse, insbesondere (tiefe) venöse Thromboembolien oder arterielle Thromboembolien, sind bei Kindern im Vergleich zur erwachsenen Population selten. Die überwiegende Mehrheit der Kinder mit Thrombose hat zum Zeitpunkt des Ereignisses eine oder mehrere damit zusammenhängende Grunderkrankungen (z. B. Infektion, Malignom, eine schwere Krankheit und/oder einen einliegenden zentralen Venenkatheter [ZVK]). Eine spontane Thrombose stellt anders als bei Erwachsenen eine sehr seltene Komplikation dar(1–4). Da Thrombosen im Kindesalter in der Regel kranke Kinder betreffen, ist eine bestehende Thrombophilie wahrscheinlich eher als zusätzlicher Risikofaktor denn als isolierte Thromboseursache zu werten(3).
Labormarker für Thrombophilie
Thrombophilie bezeichnet eine Neigung zur Bildung von Blutgerinnseln aufgrund erblicher und/oder erworbener Risikofaktoren. Die Thrombophiliediagnostik umfasst in der Regel die Laboranalyse von Hyperkoagulabilitätsmarkern, die potenziell mit einem erhöhten Thromboserisiko einhergehen. Eine Reihe von Markern für erbliche und erworbene Thrombophilie sind bekannt. Zu den Markern der hereditären Thrombophilie gehören prothrombotische Mutationen der Gene, die für Faktor V (Faktor-V-Leiden-Mutation [FVL], Variante G1691A) und für Prothrombin (Mutation des Prothrombin-Gens [PTG], Variante G20210A) kodieren, sowie ein Mangel an körpereigenen Gerinnungshemmern, insbesondere Antithrombin (AT), Protein C (PC) und Protein S (PS)(3-5,8). Zu den erworbenen Risikofaktoren zählen Antiphospholipid-Antikörper (aPL). Die Testung auf aPL ist erforderlich im Zusammenhang mit einer Thrombose und/oder anderen klinischen Merkmalen, die auf ein Antiphospholipid-Syndrom (APS) beim Indexfall hindeuten(3,5,9).
Weitere laboranalytische Risikofaktoren für Thrombosen wurden beschrieben, sind jedoch nicht allgemein anerkannt. Konkret geht es um erhöhte Werte von Gerinnungsfaktoren (insbesondere Faktor VIII)(10), Homocystein und/oder Lipoprotein (a)(5). Ihre Bedeutung hinsichtlich des Risikos thromboembolischer Komplikationen bei Kindern ist jedoch nach wie vor unklar, und wir raten von der systematischen Durchführung dieser Tests im Rahmen der Thrombophiliediagnostik bei Kindern angesichts mangelnder Empfehlungen zur therapeutischen Relevanz auffälliger Ergebnisse bei dieser Population ab(3). Das Screening auf Mutationen (Polymorphismen) der Methylentetrahydrofolat-Reduktase (MTHFR) sollte nicht mehr Teil der Thrombophiliediagnostik sein(11).
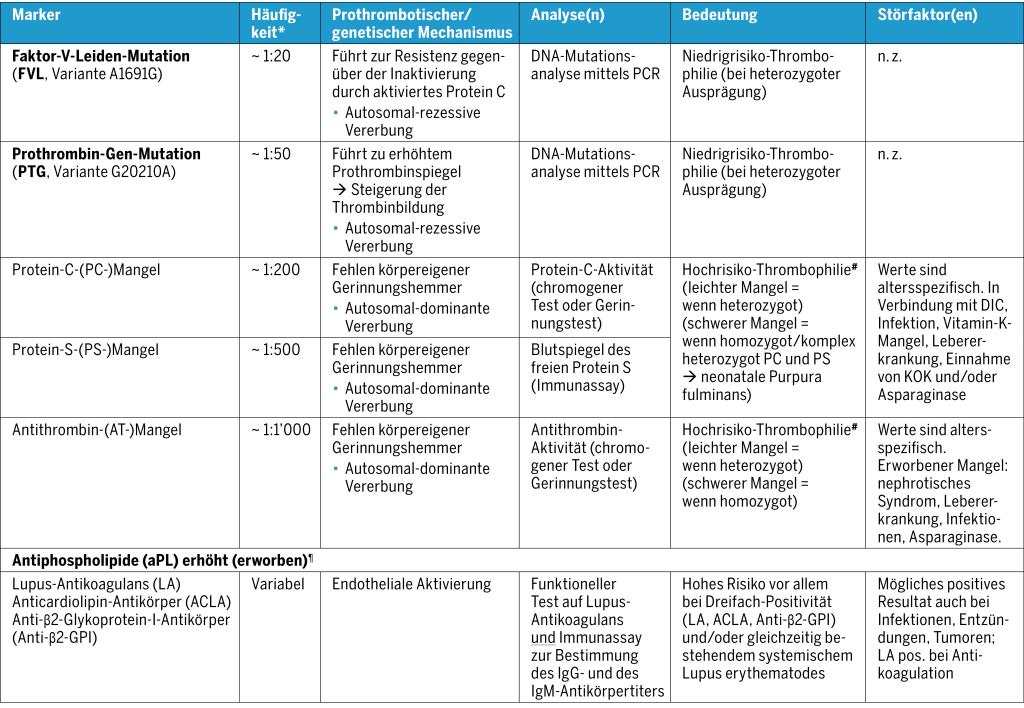
Die im Screening-Panel für Thrombophilie enthaltenen Marker, ihr Wirkmechanismus, ihre Analyse und weitere Merkmale sind in Tabelle 1 aufgeführt. Die berichtete Häufigkeit der einzelnen Thrombophiliemerkmale in der Allgemeinbevölkerung (s. Tabelle 1) kann je nach Markertyp (von 5 % für die FVL-Mutation bis 1:1000 für AT-Mangel) sowie teils in Abhängigkeit von der ethnischen Herkunft der Population variieren(3, 5, 12, 13).
Teilweise liegen Studien und Berichte zum möglichen Einfluss eines Thrombophiliemerkmals auf das Risiko einer erstmaligen Venenthrombose, eines Rezidivs, eines Schlaganfalls (ZVI) oder einer peripheren (nichtzerebralen) arteriellen Thrombose bei Kindern vor(4,14-19). Insgesamt war das Risiko eines erstmaligen oder rezidivierenden venös-thrombotischen Ereignisses bei Personen mit AT-, CP- oder PS-Mangel und/oder homozygoten / komplex heterozygoten FVL- oder PTG-Mutationen (Hochrisiko-Thrombophiliemerkmal) am höchsten. Personen mit heterozygoter FVL- oder PTG-Mutation wiesen hingegen ein geringeres Risiko auf (Niedrigrisiko-Thrombophiliemerkmal)(3,20). Bei Kindern war die Prävalenz eines Thrombophiliemerkmals beim ischämischen ZVI, nicht jedoch beim perinatalen ischämischen ZVI, höher als in der Kontrollgruppe(21–23). Der Einfluss von Thrombophilie-Markern auf nichtzerebrale arterielle thromboembolische Ereignisse ist weniger klar(4).
Ansatz bei der Thrombophiliediagnostik
Thromboembolische Ereignisse im Kindesalter treten vorwiegend bei kranken Kindern in stationärer Umgebung auf. Ihre Versorgung, einschliesslich aller Entscheidungen betreffend Thrombophilie-Tests, obliegt häufig den Spitalärzt:innen. Niedergelassene Kinderärzt:innen dagegen können im Rahmen einer ambulanten Konsultation mit der elterlichen Frage konfrontiert sein, was angesichts einer positiven Familienanamnese für thromboembolische Ereignisse und/oder Thrombophilie zu unternehmen sei. Idealerweise sollten sie die Patient:innen und ihre Familien vor einer eventuellen Abklärung zur fundierten Beratung an eine Kinderhämatologin oder einen Kinderhämatologen überweisen(3). Angesichts der eingeschränkten Datenlage stützen sich die Empfehlungen zur Thrombophiliediagnostik bei Kindern und Jugendlichen praktisch grösstenteils auf Expertenmeinungen und sind daher im Rahmen einer fachärztlichen Konsultation im Einzelfall zu erörtern.
Insgesamt umfassen die Szenarien, bei denen eine Thrombophiliediagnostik bei Kindern infrage kommt(1, 24):
- pädiatrische Patient:innen mit bereits stattgehabtem thrombotischem Ereignis (Indexfall) sowie
- nicht betroffene (asymptomatische) Kinder/Jugendliche mit oder ohne positive Familienanamnese für Thrombosen (vor allem Verwandte ersten Grades).
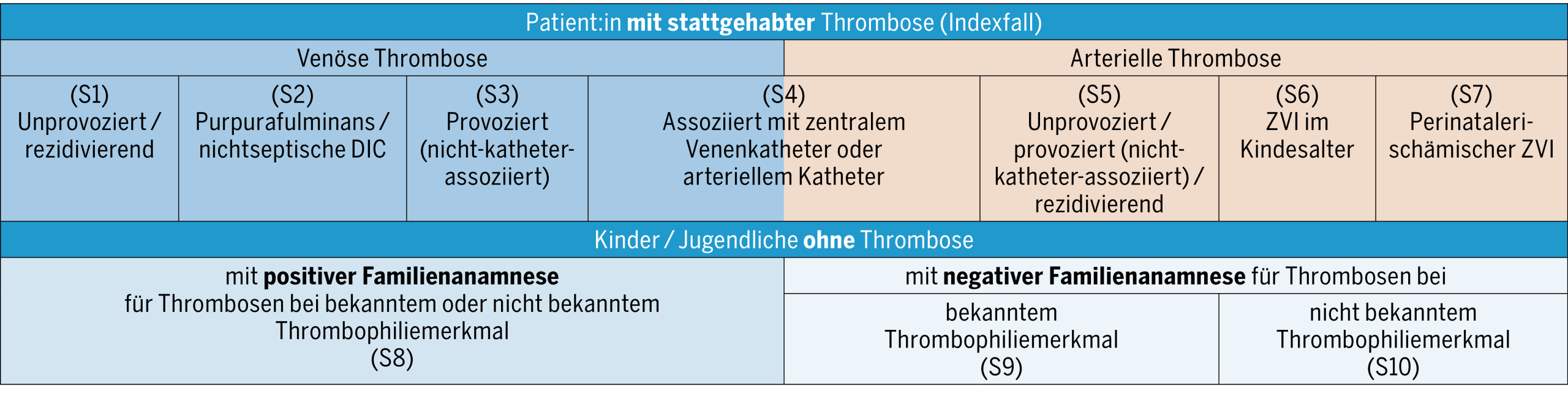
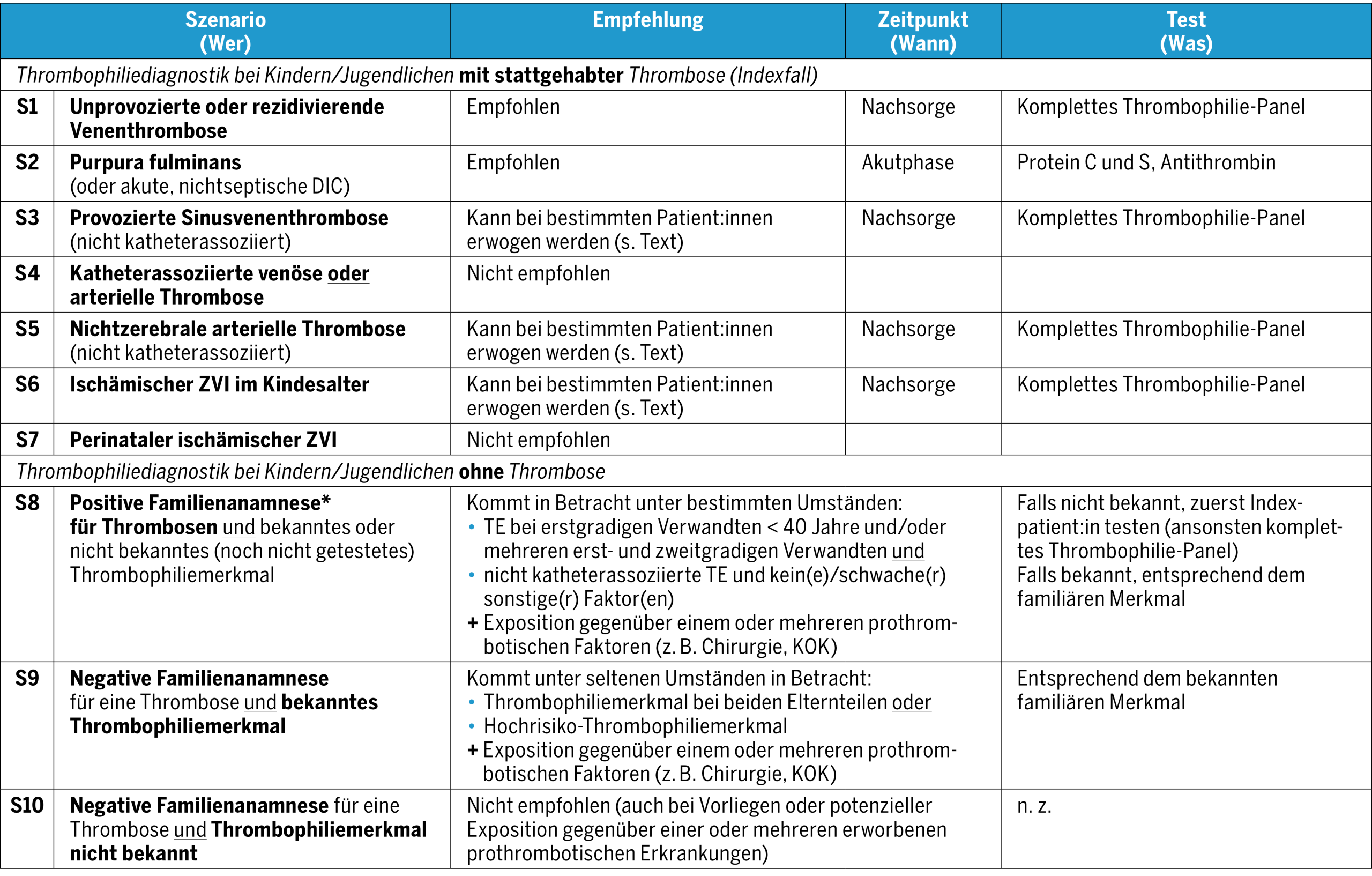
Die Beurteilung konzentriert sich auf drei Hauptaspekte. Zunächst einmal geht es darum, den Nutzen des Screenings in einem bestimmten Kontext zu bestimmen (Wer). Zweitens gilt es, den geeigneten Zeitpunkt für die Durchführung festzulegen (Wann). Wird eine entsprechende Notwendigkeit festgestellt, sind die durchzuführenden Tests zu bestimmen (Was). Zur Orientierung geben nachstehend Abbildung 1 und Tabelle 2 einen Überblick über die Szenarien (S1 bis S10) und die entsprechenden Empfehlungen zur Abklärung.
Mögliche Argumente für eine Thrombophiliediagnostik können unter anderem sein:
- Erkenntnisgewinn zur Pathophysiologie des Ereignisses
- Einschätzung des Rezidivrisikos im jeweiligen Fall
- Sensibilisierung für die pharmakologische Thromboseprophylaxe in Hochrisikosituationen (Operation, schwere Erkrankung, Trauma)
- Orientierungshilfe für die Anwendung kombinierter oraler Kontrazeptiva
Andererseits sind auch mögliche Argumente gegen ein Screening zu berücksichtigen, z. B.:
- Die Seltenheit von Thrombosen im Kindesalter und der meist bestehende Zusammenhang mit erworbenen Faktoren
- Bereits bekanntes klinisches Risiko mit indizierter Sekundärprophylaxe
- Risiko von Fehlinterpretationen der Ergebnisse bzw. des Wiegens in falscher Sicherheit
- Informationen zur familiären Belastung auch ohne weitere Tests ermittelbar
- Ethische Fragen bei Gentests an Kindern; diese Tests sollten sich auf Situationen beschränken, in denen eine frühzeitige Intervention die Prognose verbessert(3, 25)
Zu beachten ist, dass auffällige Ergebnisse in nicht-DNA-basierten Tests (unter anderem Tests auf Protein C und S sowie Antithrombin), die altersspezifischen und durch erworbene Erkrankungen bedingten Einflüssen unterliegen könnten (siehe Tabelle 1), grundsätzlich einer Bestätigung bedürfen. Darüber hinaus empfiehlt es sich, auch beide Elternteile zu testen, bevor die Diagnose eines hereditären Mangels an Protein C, Protein S oder Antithrombin gestellt wird.
Thrombophiliediagnostik bei Patient:innen nach einem thromboembolischen Ereignis (Indexfall):
Die berichtete Prävalenz der verschiedenen Thrombophilie-Merkmale bei pädiatrischen Thrombose-Patient:innen kann zwischen 13 % und 79 % variieren, was in erster Linie bedingt ist durch unterschiedliche Studiendesigns sowie klinische und demographische Merkmale der Studienpopulationen(3). Grundsätzlich gilt es, die Umstände zu verstehen, unter denen das thrombotische Ereignis aufgetreten ist, und die Thrombophilie-Testresultate mit Blick auf eine eventuelle therapeutische Relevanz vor diesem Hintergrund einzuordnen.
Nachfolgend sind Thrombophilie-Testempfehlungen für unterschiedliche Szenarien (S1–S7) bei Thrombosepatient:innen (Abbildung 1, Tabelle 2) aufgeführt:
- Bei der unprovozierten oder rezidivierenden venösen Thrombose bei Neugeborenen, Kindern und Jugendlichen (S1) wird die Testung auf Thrombophilie empfohlen. Hintergrund: Unprovozierte (spontane) Venenthrombosen sind in der Pädiatrie extrem selten, bei relativ hoher Rezidivrate, was durch eine zugrunde liegende Thrombophilie bedingt sein kann(3, 14, 19, 26). Eine hereditäre Thrombophilie war bei älteren Kindern mit unprovozierter VTE häufiger (60 %) als bei Kindern mit VTE infolge einer Grunderkrankung (< 10 %)(12). Die Ergebnisse können helfen, über die Dauer der Behandlung zu entscheiden und möglicherweise auch über die Notwendigkeit, Angehörige zu testen, insbesondere im Zusammenhang mit einem Hochrisiko-Thrombophiliemerkmal (Definition siehe Einleitung).
- Bei Neugeborenen mit Purpura fulminans (S2) (oder anderen unprovozierten schweren Thrombosen, etwa ausgedehnten Sinusvenenthrombosen) sind sofortige Thrombophilie-Tests dringend angeraten, um Merkmale einer Hochrisiko-Thrombophilie, insbesondere einen schweren (homozygoten / komplex heterozygoten) Mangel an Protein S, C und Antithrombin, abzuklären. Hintergrund: Hier ist rasch eine Substitutionstherapie einzuleiten (27, 28). In solchen Fällen wird dringend empfohlen, ein auf die Behandlung von Thrombosen spezialisiertes Zentrum zu konsultieren.
- Bei einer provozierten (nicht ZVK-assoziierten) Venenthrombose (S3) bei Neugeborenen, Kindern und Jugendlichen wird in der Regel keine Thrombophiliediagnostik empfohlen, sie kann aber unter bestimmten Umständen in Betracht gezogen werden. Hintergrund: Die Datenlage ist stark eingeschränkt und die Praktiken können sehr unterschiedlich sein. Bei Patient:innen mit erstmaliger Venenthrombose in Verbindung mit einer eindeutigen Erkrankung/Situation (z. B. schwere systemische Infektion, Krebs/Begleittherapie, grössere Operation/Trauma, nephrotisches Syndrom) wird keine Abklärung empfohlen. Dies auch auf der Grundlage, dass die Auslöser in den meisten Fällen passager sind und die Behandlungsdauer bei einer provozierten Venenthrombose in der Regel ≤ 3 Monate beträgt(1). Unter bestimmten Umständen, etwa bei ungewöhnlichen thrombotischen Ereignissen und/oder nicht eindeutigen bzw. schwachen auslösenden Faktoren, können Thrombophilie-Tests jedoch sinnvoll sein(14, 20).
- Bei einer venösen oder arteriellen Thrombose im Zusammenhang mit einem ZVK bzw. einem arteriellen Katheter (AK) bei Neugeborenen, Kindern oder Jugendlichen (S4) werden Thrombophilie-Tests nicht empfohlen. Hintergrund: Ein einliegender Katheter ist der wichtigste Risikofaktor für Thrombosen bei Kindern; Thrombophilie-Tests haben hier keinerlei Einfluss auf Therapieentscheidungen(4, 29, 30).
- Bei unprovozierten oder provozierten (nicht katheterassoziierten) nichtzerebralen arteriellen Thrombosen (S5) kann bei ungewöhnlichen thrombotischen Ereignissen und/oder unklaren auslösenden Faktoren eine Abklärung in Betracht gezogen werden. Hintergrund: Diese Komplikation tritt selten auf und ist mit bestimmten Krankheiten assoziiert, z. B. Gefässfehlbildungen, bestimmten Arteriitiden (z. B. beim Kawasaki-Syndrom, Takayasu-Arteriitis) oder familiärer Hyperlipidämie. Zudem lässt die nur spärliche Datenlage keine definitive Empfehlung zu(2, 4).
- Beim ischämischen Schlaganfall (ZVI) im Kindesalter (S6) kann in Abhängigkeit von den Umständen des Auftretens eine Thrombophilie-Abklärung erwogen werden (ausgenommen bei Kindern mit Sichelzellanämie)(21, 31). Hintergrund: Die derzeitige Datenlage deutet auf einen Zusammenhang zwischen labormedizinisch diagnostizierter (hereditärer oder erworbener) Thrombophilie und dem Auftreten eines ischämischen ZVI hin(18). Angesichts der vielfältigen Situationen, in denen ein ZVI auftreten kann, sind diese Daten jedoch nicht hinreichend, um den Nutzen der Tests zu belegen. Zudem ist der Einfluss einer Thrombophilie auf das Risiko von ZVI-Rezidiven weniger eindeutig(17, 18, 21, 31).
- Bei ischämischem ZVI in der Perinatalperiode (S7) werden Thrombophilie-Tests nicht empfohlen. Gegenwärtig gibt es keine Daten, die eine systematische Durchführung dieser Tests ausserhalb von Forschungsstudien rechtfertigen. Welche Bedeutung die Thrombophilie in der Pathophysiologie und hinsichtlich der Langzeitergebnisse von perinatalen ZVI hat, ist noch ungeklärt(23,32).
Bei der Wahl des Testzeitpunkts sind die möglichen Auswirkungen der Tests auf die Versorgung des Kindes zu berücksichtigen. Bei akuten thrombotischen Ereignissen werden Thrombophilie-Tests bis auf wenige Ausnahmen nicht empfohlen, da die Testergebnisse nur selten einen Einfluss auf die Akutbehandlung von Thrombosebetroffenen haben. Eine Ausnahme bilden Neugeborene mit Purpura fulminans (schwerer Protein-S-Mangel), bei denen rasch eine Substitutionstherapie eingeleitet werden muss(27, 28). Ferner ist bei dringendem Verdacht auf APS ein Test auf aPL noch vor Beginn der Antikoagulation zu erwägen, um eine Ergebnisverzerrung zu vermeiden.
Beim Grossteil der Fälle sollte die diagnostische Abklärung – sofern eine Indikation besteht – bis zu einem Mindestalter von 3 bis 6 Monaten sowie bis nach dem Absetzen der Antikoagulationstherapie zurückgestellt werden. Die Ergebnisse können zur Einschätzung des Rückfallrisikos beitragen und als Orientierungshilfe für die Behandlungsdauer oder die Sekundärprophylaxe in Risikosituationen dienen.
Angesichts der Datenlage kann den Patient:innen und ihren Angehörigen allerdings noch kein endgültiger risikobasierter Ansatz empfohlen werden(1).
Thrombophilie-Abklärung bei Patient:innen ohne anamnestisch bekannte Thrombosen (asymptomatische Patient:innen):
Die Entscheidung über eine eventuelle Abklärung richtet sich bei dieser Konstellation vor allem danach, ob es in der Familie bereits Fälle von Thrombosen gab, und in geringerem Masse danach, ob ein Thrombophiliemerkmal innerhalb der Familie vorliegt.
Diagnostik bei Kindern/Jugendlichen mit positiver Familienanamnese für Thrombosen (S8):
Bei Kindern/Jugendlichen mit einer positiven Familienanamnese für Thrombosen und bekanntem oder nicht bekanntem (noch nicht getestetem) Thrombophiliemerkmal wird eine Abklärung nicht grundsätzlich empfohlen, kann aber unter Umständen in Betracht kommen. Hintergrund: Zur Prävalenz von (hauptsächlich venösen) Thrombosen bei Kindern mit positiver Familienanamnese und zum Vorliegen eines Thrombophiliemerkmals bei dieser Konstellation liegen nur eingeschränkte, vorwiegend von Erwachsenendaten abgeleitete Angaben vor(3, 20).
Obgleich hier die Meinungen auseinandergehen, kann eine Abklärung in bestimmten Situationen sinnvoll sein, insbesondere bei entsprechender familiärer Vorgeschichte, etwa einer nicht katheterassoziierten Thrombose in Verbindung mit schwachen (z. B. «Pille») oder nicht bekannten auslösenden Faktoren bei einem Verwandten ersten Grades vor Vollendung des 40. Lebensjahres oder bei mehreren nahen Verwandten. Es ist daher sehr wichtig, die Umstände der bei den Indexpatient:innen der Familie stattgehabten Thrombosen zu eruieren, insbesondere die Risikofaktoren, die gesundheitlichen Rahmenbedingungen und das Alter bei Eintritt der thrombotischen Komplikation. Überdies treten Venenthrombosen häufiger bei Träger:innen von Thrombophilie-Determinanten auf, vorwiegend einem Mangel an Antithrombin, Protein C oder Protein S (jährliche Inzidenz: 2,82 %), als bei Vorliegen von Niedrigrisiko-Merkmalen (heterozygote FVL- oder PTG-Mutation; 0,2–0,5 %/Jahr)(3, 14, 15). Erscheint eine Abklärung angezeigt, sollte sie daher zunächst bei den Indexpatient:innen und anschliessend bei ihren asymptomatischen Angehörigen ohne thrombotische Komplikationen erfolgen und vor allem auf den Nachweis von Hochrisiko-Merkmalen gerichtet sein.
Bei Kindern/Jugendlichen ohne positive Familienanamnese für Thrombosen:
- Bei bekanntem Thrombophiliemerkmal in der Familie wird die Abklärung nicht grundsätzlich empfohlen (S9), sondern kann in seltenen Fällen in Erwägung gezogen werden. Hintergrund: Die absolute Inzidenz von Thrombosen bei Kindern mit Thrombophiliemerkmal, insbesondere vom Niedrigrisiko-Typ (heterozygote FVL- oder PTG-Mutation), ist grundsätzlich niedrig. Wenngleich unter Fachleuten kein einstimmiger Konsens darüber besteht, kann eine Abklärung unter bestimmten Umständen in Betracht kommen, z. B. beim Vorliegen von Hochrisiko-Thrombophilie-Markern (siehe oben) und/oder wenn beide Elternteile ein bestimmtes Thrombophiliemerkmal tragen (mit Risiko der entsprechenden homo- oder heterozygoten Merkmalsausprägung bei den Nachkommen) sowie bei möglicher Exposition gegenüber einem thrombotischen Risiko. Zum Beispiel kann bei Mädchen aus Familien mit thrombophilen Hochrisiko-Merkmalen vor der Gabe von KOK eine Abklärung erwogen werden, um im Falle eines positiven Ergebnisses von östrogenhaltigen Kontrazeptiva abzusehen. Vorzugsweise sollte die Abklärung jedoch zurückgestellt werden, bis die Betroffenen selbst in der Lage sind, Vor- und Nachteile für sich abzuwägen(3, 20).
- Ist kein Thrombophiliemerkmal bekannt, werden in diesem Fall keine Tests empfohlen (S10). Hintergrund: Es gibt keine klinischen Studien, welche ihre Effektivität und das Nutzen-Risiko-Verhältnis einer Thromboseprophylaxe oder den Nutzen in Bezug auf die Entscheidung für ein KOK belegen(5).
Insgesamt erscheint es im Hinblick auf den geeigneten Zeitpunkt einer gegebenenfalls erforderlichen Abklärung sinnvoll, bei asymptomatischen Kindern abzuwarten, bis sie nach Abwägung der Vor- und Nachteile selbst darüber entscheiden können. Dies gilt insbesondere, da die absolute Inzidenz von Thrombosen im Kindesalter selbst bei Vorliegen eines thrombophilen Merkmals sehr gering ist. Tatsächlich ist eine Abklärung in diesem Zusammenhang angesichts der oben genannten Vor- und Nachteile möglicherweise nicht gerechtfertigt(3). Bei asymptomatischen Kindern sollten nur Tests auf die gut untersuchten genetisch bedingten Thrombophilien erfolgen, die in Tabelle 1 zusammengefasst sind. Bei nicht bekanntem familiärem Thrombophiliemerkmal kommt zunächst die Testung des Index-Familienmitglieds mit TE in Betracht. Bei bekanntem Thrombophiliemerkmal wird empfohlen, selektiv darauf zu testen.
Schlussfolgerung
Thrombotische Komplikationen bei Kindern sind selten und treten vorwiegend dann auf, wenn zum Zeitpunkt der Komplikation mehrere Risikofaktoren/Begleiterkrankungen vorliegen. Eine bestehende Thrombophilie ist wahrscheinlich eher als zusätzlicher Risikofaktor denn als isolierte Thromboseursache zu werten(3). Die Entscheidung, ob, wann und welche Tests beim jeweiligen Kind angemessen sind, obliegt der behandelnden Ärztin bzw. dem behandelnden Arzt. In jedem Fall ist es ratsam, die Thrombophiliediagnostik mit den Patient:innen und ihren Angehörigen eingehend zu erörtern und die Empfehlung dazu nur nach Rücksprache mit einer Spezialistin bzw. einem Spezialisten auszusprechen.
Referenzen
- Monagle P, Azzam M, Bercovitz R, Betensky M, Bhat R, Biss T, et al. American Society of Hematology/International Society on Thrombosis and Haemostasis 2024 updated guidelines for treatment of venous thromboembolism in pediatric patients. Blood Adv. 2025;9(10):2587-2636.
- Rizzi M, Albisetti M. Treatment of arterial thrombosis in children: Methods and mechanisms. Thromb Res. 2018;169:113-119.
- Nowak-Gottl U, van Ommen H, Kenet G. Thrombophilia testing in children: What and when should be tested? Thromb Res. 2018;164:75-78.
- Rizzi M CAK, Bosch A., Albisetti M Arterial Thrombosis. In: Blanchette VS BL, Carcao MD, Kumar R, Rand ML, Revel-Vilk S editor. SickKids Handbook of Pediatric Thrombosis and Hemostasis, ed 3, rev and ext S.Karger AG, Basel; 2024. p. pp275-287.
- Sabapathy C. AA, Kumar R., Avila L., Van Ommen C.H. Diagnostic Approach to Thrombosis and Thrombophilia In: Blanchette VS BL, Carcao MD, Kumar R, Rand ML, Revel-Vilk S editor. SickKids Handbook of Pediatric Thrombosis and Hemostasis (3rd, revised and extended edition): S.Karger AG, Basel; 2024. p. 233–255.
- Kumar R, Bakeer N, Dawson J, Al-Mughairy A, Stanek J, Dunn A, et al. Impact of SERPINC1 mutation on thrombotic phenotype in children with congenital antithrombin deficiency-first analysis of the International Society on Thrombosis and Haemostasis pediatric antithrombin deficiency database and biorepository. J Thromb Haemost. 2023;21(5):1248-1257.
- Marlar RA, Gausman JN, Tsuda H, Rollins-Raval MA, Brinkman HJM. Recommendations for clinical laboratory testing for protein S deficiency: Communication from the SSC committee plasma coagulation inhibitors of the ISTH. J Thromb Haemost. 2021;19(1):68-74.
- Cooper PC, Pavlova A, Moore GW, Hickey KP, Marlar RA. Recommendations for clinical laboratory testing for protein C deficiency, for the subcommittee on plasma coagulation inhibitors of the ISTH. J Thromb Haemost. 2020;18(2):271-277.
- Vandevelde A, Chayoua W, de Laat B, Moore GW, Musial J, Zuily S, et al. Added value of antiphosphatidylserine/prothrombin antibodies in the workup of thrombotic antiphospholipid syndrome: Communication from the ISTH SSC Subcommittee on Lupus Anticoagulant/Antiphospholipid Antibodies. J Thromb Haemost. 2022;20(9):2136-2150.
- Bosch A, Uleryk E, Avila L. Role of factor VIII, IX, and XI in venous thrombosis recurrence risk in adults and children: A systematic review. Res Pract Thromb Haemost. 2023;7(2):100064.
- Deloughery TG, Hunt BJ, Barnes GD, Connors JM, Committee WTDS. A call to action: MTHFR polymorphisms should not be a part of inherited thrombophilia testing. Res Pract Thromb Haemost. 2022;6(4):e12739.
- Revel-Vilk S, Chan A, Bauman M, Massicotte P. Prothrombotic conditions in an unselected cohort of children with venous thromboembolic disease. J Thromb Haemost. 2003;1(5):915-921.
- van Ommen CH, Heijboer H, van den Dool EJ, Hutten BA, Peters M. Pediatric venous thromboembolic disease in one single center: congenital prothrombotic disorders and the clinical outcome. J Thromb Haemost. 2003;1(12):2516-2522.
- Klaassen IL, van Ommen CH, Middeldorp S. Manifestations and clinical impact of pediatric inherited thrombophilia. Blood. 2015;125(7):1073-1077.
- Holzhauer S, Goldenberg NA, Junker R, Heller C, Stoll M, Manner D, et al. Inherited thrombophilia in children with venous thromboembolism and the familial risk of thromboembolism: an observational study. Blood. 2012;120(7):1510-1515.
- Nowak-Gottl U, Kurnik K, Manner D, Kenet G. Thrombophilia testing in neonates and infants with thrombosis. Semin Fetal Neonatal Med. 2011;16(6):345-348.
- Kenet G, Aronis S, Berkun Y, Bonduel M, Chan A, Goldenberg NA, et al. Impact of persistent antiphospholipid antibodies on risk of incident symptomatic thromboembolism in children: a systematic review and meta-analysis. Semin Thromb Hemost. 2011;37(7):802-809.
- Kenet G, Lutkhoff LK, Albisetti M, Bernard T, Bonduel M, Brandao L, et al. Impact of thrombophilia on risk of arterial ischemic stroke or cerebral sinovenous thrombosis in neonates and children: a systematic review and meta-analysis of observational studies. Circulation. 2010;121(16):1838-1847.
- Young G, Albisetti M, Bonduel M, Brandao L, Chan A, Friedrichs F, et al. Impact of inherited thrombophilia on venous thromboembolism in children: a systematic review and meta-analysis of observational studies. Circulation. 2008;118(13):1373-1382.
- Middeldorp S, Nieuwlaat R, Baumann Kreuziger L, Coppens M, Houghton D, James AH, et al. American Society of Hematology 2023 guidelines for management of venous thromboembolism: thrombophilia testing. Blood Adv. 2023;7(22):7101-7138.
- Maher K, Persa L, Barry D, Lee-Eng J, Dichek H, Joshi S, et al. Thrombophilia screening in the routine clinical care of children with arterial ischemic stroke. Pediatr Blood Cancer. 2023;70(8):e30381.
- Kumar R, Sun LR, Rodriguez V, Sankar A, Sharma M, Meoded A, et al. Hemostatic and Thrombotic Considerations in the Diagnosis and Management of Childhood Arterial Ischemic Stroke: A Narrative Review. Semin Pediatr Neurol. 2022;43:101003.
- Saliba E, Debillon T, Recommandations accident vasculaire cerebral n, Auvin S, Baud O, Biran V, et al. [Neonatal arterial ischemic stroke: Review of the current guidelines]. Arch Pediatr. 2017;24(2):180-188.
- Stevens SM, Woller SC, Bauer KA, Kasthuri R, Cushman M, Streiff M, et al. Guidance for the evaluation and treatment of hereditary and acquired thrombophilia. J Thromb Thrombolysis. 2016;41(1):154-164.
- Thornburg CD, Dixon N, Paulyson-Nunez K, Ortel T. Thrombophilia screening in asymptomatic children. Thromb Res. 2008;121(5):597-604.
- Whitworth H, Clark HH, Hubbard RA, Witmer C, Leonard CE, Raffini L. High rate of recurrent venous thromboembolism in children and adolescents with unprovoked venous thromboembolism. J Thromb Haemost. 2023;21(1):47-56.
- Minford A, Brandao LR, Othman M, Male C, Abdul-Kadir R, Monagle P, et al. Diagnosis and management of severe congenital protein C deficiency (SCPCD): Communication from the SSC of the ISTH. J Thromb Haemost. 2022;20(7):1735-1743.
- Price VE, Ledingham DL, Krumpel A, Chan AK. Diagnosis and management of neonatal purpura fulminans. Semin Fetal Neonatal Med. 2011;16(6):318-322.
- O’Brien SH, Badawy SM, Rotz SJ, Shah MD, Makarski J, Bercovitz RS, et al. The ASH-ASPHO Choosing Wisely Campaign: 5 hematologic tests and treatments to question. Blood Adv. 2022;6(2):679-685.
- Neshat-Vahid S, Pierce R, Hersey D, Raffini LJ, Faustino EV. Association of thrombophilia and catheter-associated thrombosis in children: a systematic review and meta-analysis. J Thromb Haemost. 2016;14(9):1749-1758.
- Powers WJ, Rabinstein AA, Ackerson T, Adeoye OM, Bambakidis NC, Becker K, et al. Guidelines for the Early Management of Patients With Acute Ischemic Stroke: 2019 Update to the 2018 Guidelines for the Early Management of Acute Ischemic Stroke: A Guideline for Healthcare Professionals From the American Heart Association/American Stroke Association. Stroke. 2019;50(12):e344-e418.
- Curtis C, Mineyko A, Massicotte P, Leaker M, Jiang XY, Floer A, et al. Thrombophilia risk is not increased in children after perinatal stroke. Blood. 2017;129(20):2793-2800.
Weitere Informationen
Autor:innen
-
PD Dr med. et phil. Mattia RizziMédecin Associé, Unité d’Hématologie-Oncologie, Service de Pédiatrie, Hôpital des Enfants, CHUV, Lausanne
