L’impact des infections des voies respiratoires, d’allergies et de facteurs environnementaux sur la santé des enfants : liens et approches préventives
Lead
Les infections virales des voies respiratoires sont fréquentes pendant l’enfance et sont exacerbées par des facteurs environnementaux tels les pollens, la pollution de l’air et le réchauffement climatique. Des mesures préventives deviennent de plus en plus importantes, e.a. la prévention primaire et secondaire par des lysats bactériens.
Abstract
Pendant l’enfance les infections de voies respiratoires (IVR) sont la plupart des fois virales. Elles se manifestent surtout pendant l’hiver mais peuvent être intensifiées en dehors de la saison froide par des facteurs environnementaux comme les pollens, la pollution de l’air et le réchauffement climatique. Des études récentes montrent que la présence de pollen dans l’air peut augmenter le risque d’IVR aussi sans anamnèse d’allergie. Se pose donc la question s’il n’est pas raisonnable de procéder, chez les patient·e·s à risque, enfants avec des IVR fréquentes, allergies ou asthme, à une prévention des infections pendant toute l’année. La prévention des IVR et l’atténuation de leurs symptômes sont des questions pertinentes qui pourraient prendre encore plus d’importance suite au changements climatiques et à la détérioration de la qualité de l’air. Dans cet article nous abordons les liens entre IVR, allergies et facteurs environnementaux et décrivons de possibles stratégies de prévention pendant l’enfance.
Introduction
Les personnes avec de l’asthme ou une bronchopneumopathie chronique obstructive (BPCO) ont un risque élevé de souffrir de symptômes sévères ou prolongés lors d’une IVR ; d’autre part l’IVR peut déclencher une exacerbation de la BPCO ou des crises d’asthme(1,2,3). On estime que les virus respiratoires, notamment influenza, VRS et rhinovirus, sont responsables de plus de 85% des crises d’asthme(4). Les enfants encourent globalement un risque élevé de contracter une infection pulmonaire virale et sont particulièrement sensibles à la combinaison pollution de l’air, allergie et infections respiratoires, qui devient un problème croissant mondialement(5,6). Des IVR sévères avant l’âge de 5 ans comptent parmi les facteurs qui augmentent le risque de développer une BPCO plus tard à l’âge adulte(7,8).
Infections, facteurs environnementaux et rôle des allergies
Des facteurs environnementaux peuvent exacerber la sensibilité aux IVR. Certains, p.ex. la pollution de l’air par des allergènes aérogènes (e.a. excréments d’acariens), sont présents toute l’année, l’exposition aux allergènes saisonniers étant également significative. Les pollens peuvent inhiber l’expression d’interféron α, β et λ, qui jouent un rôle central dans la réponse immunologique antivirale(10). De plus, les pollens véhiculent souvent des polluants aériens et des germes pathogènes, surtout des virus(11). Fatalement existe un lien entre pollution de l’air et charge pollinique, dû au changement resp. réchauffement climatique qui influence fortement l’aérobiologie et notamment la présence de pollens. Avec le réchauffement, il faut s’attendre à un allongement de la saison pollinique (début précoce, durée plus longue) et une plus forte production de pollen (climat globalement plus chaud, excès de CO2 dans l’atmosphère, phases de stress pour les plantes produisant des pollens, années riches en pollens plus fréquentes). Les changements climatiques engendreront en outre une modification des conditions de croissance, avec un déplacement des zones de végétation des plantes produisant des pollens(12). La zone de végétation de l’ambroisie p.ex. se déplace de plus en plus vers le pôle, la charge en pollen deviendra donc conséquente aussi dans les latitudes tempérées.
En outre les changements climatiques, la pollution de l’air et les modifications de l’aérobiologie mentionnés influencent directement les manifestations allergiques par un effet sur la barrière épithéliale respectivement sa disruption, à travers la réponse, ou le renforcement de la réponse, des lymphocytes T helper de type 2 (Th2) ainsi que par des mécanismes épigénétiques comme la modification de la méthylation de gènes immunomodulateurs, e.a. FOXP3, IL4, IL10 et IFNG(12). De plus les pollens contiennent, comme les excréments d’acariens, des protéases qui affectent directement la membrane épithéliale(13). C’est cet impact de la pollution de l’air sur l’intégrité de la fonction de barrière des muqueuses respiratoires, e.a. par stress oxydatif, expression réduite de protéines tight junction et production accrue de cytokines pro-inflammatoires, qui permet à des allergènes ou virus de s’infiltrer plus facilement et provoquer des réactions inflammatoires(12,14,15). Il peut alors se développer un cercle vicieux entre dysbiose (modification du microbiome local avec une plus forte colonisation par des germes opportunistes), déplacement, dans le cadre d’une IVR, de germes pathogènes dans des couches tissulaires plus profondes, réaction immunitaire et inflammatoire conséquente et finalement guérison compromise des lésions de la muqueuse(16).
La réduction des fonctions de défense épithéliales est un facteur de plus accentuant le risque d’IVR pour les personnes allergiques. Cela se manifeste tôt dans la vie. Chez les nourrissons qui développent plus tard une atopie ou une allergie manifeste, le développement et la maturation de la réponse immunitaire est retardée. Les biais de la réponse immunitaire Th2 avec développement retardé de la réponse des lymphocytes T helper type 1 (Th1), initialement inhérents à tous les nourrissons, sont renforcés en présence d’une prédisposition à l’atopie(17). En résulte une réponse immunitaire Th1 moins efficace et p.ex. une production moindre d’interféron gamma (IFN-γ) dans le cadre d’une réponse immunitaire antivirale lors d’une IVR. Cette combinaison entre réponse immunitaire Th1 initialement moins efficace et retard du développement d’une réponse immunitaire focalisée et performante conditionne e.a. la récurrence d’IVA virales chez les personnes atopiques déjà tôt dans la vie(12). Des facteurs environnementaux peuvent donc favoriser les IVR pendant toute l’année par des mécanismes qui ne sont pas forcément liés ou déclenchés par une atopie ou des maladies allergiques des voies respiratoires mais sont renforcés par leur présence.
De études récentes montrent en outre que des polluants de l’air n’affaiblissent, dans le cadre des mécanismes mentionnés, pas seulement la défense antivirale mais décalent aussi la balance entre réponse immunitaire Th1 et Th2. Cela favorise les inflammations allergiques mais peut aussi, indépendamment des facteurs susmentionnés, impacter la défense antivirale par la réduction de la production d’interféron (p.ex. IFN-γ)(6). Chez les enfants avec une infection à VRS ou rhinovirus a été observée une plus forte réplication virale due à un trouble de la barrière épithéliale et une production réduite d’interféron, avec pour conséquence l’apparition ou l’accentuation de symptômes allergiques(2). Les infections virales pendant la petite enfance sont entre temps considérées comme étant un facteur de risque pour le développement de maladies chroniques des voies respiratoires comme l’asthme, d’autant plus en conjonction avec une prédisposition génétique et la pollution de l’air, qui impacte, en synergie avec les infections virales, la muqueuse respiratoire avec potentiellement des effets à long terme sur la santé.
Pics synchrones
Une des situations les mieux documentées, ayant causé une hausse d’IVR en lien avec le pollen, a été la pandémie Covid-19. Notamment en Suisse on a constaté une corrélation temporelle entre le nombre d’infections SARS-Cov-2 et les pics de pollen, donc l’exposition au pollen(18). Cette observation n’est pourtant pas spécifique à Covid-19. Une étude sur 5 ans a mis en évidence un synchronicité entre pics de pollen et IVR chez 6’223 enfants en Corée du Sud(5), indépendamment de la présence d’une allergie (fig. 1). Le lien entre exposition au pollen et symptômes respiratoires, donc IVR, existe déjà chez le nourrisson, comme le montrent les données suisses d’une cohorte prospective de nouveau-nés en bonne santé, la cohorte Bern-Basel Infant Lung Development (BILD). L’effet de l’exposition aux pollens sur la fréquence de symptômes respiratoires était indépendant d’allergies chez la mère ou du sexe du nourrisson(20). En résumé cela signifie qu’une prévention des IVR pendant la saison pollinique pourrait être utile aussi pour les personnes non-atopiques et surtout chez les patient·e·s à risque, p.ex. avec asthme ou BPCO ou les enfants avec des IVR récurrentes.
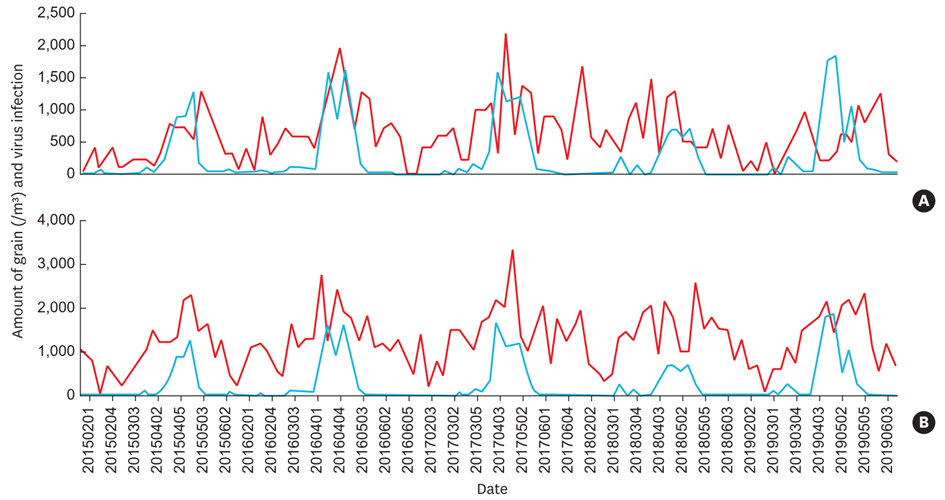
A Infections virales chez des enfants atopiques.
B Infections virales chez des enfants non-atopiques.
La ligne rouge indique le nombre de virus mis en évidence, la ligne bleu la quantité de pollen d’arbres.
Stratégies de prévention d’infections des voies respiratoires pendant l’enfance
Sont disponibles plusieurs mesures de prévention des IVR de l’enfant, qui stimulent le système immunitaire et réduisent la sensibilité aux infections. Un facteur de risque capital, clairement associé à une sensibilité accrue aux infections, est l’exposition au tabagisme. De nombreuses études prouvent que les enfants exposés à la fumée de tabac dans leur entourage souffrent plus souvent d’infections respiratoires comme les bronchites, les otites et les pneumonies(21). De plus, un style de vie sain avec une alimentation équilibrée, suffisamment de sommeil et une activité physique régulière comptent parmi les stratégies éprouvées renforçant la fonction immunitaire des enfants(22). De nombreuses études ont également examiné le rôle des micronutriments vitamine D, zinc et vitamine C. Ces éléments interviennent dans de nombreux processus immunologiques, en renforçant l’intégrité des muqueuses ou la réponse immunitaire cellulaire et par leur propriétés anti-oxydatives. Malgré leur importance biologique, des études systématiques et des méta-analyses n’ont pas révélé d’effet préventif substantiel sur les infections respiratoires aiguës de l’enfant(23,24,25). Des substances pro- ou prébiotiques, p.ex. les β-glucanes, pourraient par ailleurs aussi contribuer à la prévention d’infections, en particulier par les mécanismes du concept de l’axe intestin-poumons. Ces substances agissent potentiellement par un renforcement de l’immunité des muqueuses respiratoires. Des études livrent jusqu’ici des indices prometteurs, avec une réduction des symptômes et de la susceptibilité aux infections. Les données disponibles, notamment concernant les enfants, sont néanmoins insuffisantes pour établir des recommandations générales(26,27).
Immunomodulation par lysats bactériens, une approche complémentaire
L’immunomodulation par lysats bactériens s’impose de plus en plus en tant complément aux mesures de prévention générales, surtout pour les enfants avec des infections récurrentes ou des facteurs de risque comme l’asthme ou les atopies. Les lysats bactériens sont des lysats de plusieurs souches bactériennes, obtenues typiquement chez des patient·e·s avec des infections respiratoires récidivantes, qui stimulent le système immunitaire à plusieurs niveaux. De nombreuses données d’études précliniques ont détecté plusieurs mécanismes d’action(28), multiples et complexes, à l’image des processus immunologiques dans le poumon. La prévention par des lysats bactériens base sur la modulation de plusieurs voies de signalisation immunologiques, notamment épithéliales, dans les cellules dendritiques et les lymphocytes T régulateurs(29,30). Un des effets principaux est la stimulation de la production d’interféron α und β(31, 32), qui peuvent être inhibés, comme mentionné, par des pollens. Un autre effet important consiste à éviter une inflammation exagérée, en inhibant une série de gènes pro-inflammatoires(33,34). Les lysats bactériens modulent en plus le système immunitaire bronchique en ralentissant la réaction inflammatoire et en activant les défenses antivirales(35). L’immunomodulation par lysats bactériens renforce donc les défenses antivirales pulmonaires et améliore le contrôle de l’inflammation dans les cellules épithéliales, avec des résultats cliniques mesurables.
Effets cliniques de la prévention par lysats bactériens
De nombreuses études ont montré que les lysats bactériens induisent, chez les patient·e·s avec asthme, BPCO ou allergies et les enfants avec de fréquentes IVR virales, une réduction significative des infections respiratoires. D’après une méta-analyse Cochrane comprenant 38 études, la fréquence d’IVR chez les enfants a été réduite de 39%(36). Une méta-analyse ultérieure a aussi constaté une nette réduction de la fréquence et sévérité des crises d’asthme et wheezing en lien avec des IVR chez des enfants(37). Des résultats comparables ont été publiés concernant des personnes avec atopie et BPCO. Chez des patient·e·s âgé·e·s de 16 à 65 ans avec BPCO, asthme ou rhinite allergique, le traitement avec des lysats bactériens a diminué de manière significative le nombre d’exacerbations (fig. 2A) et d’infections des voies respiratoires (env. 33% resp. 29%) (fig. 3A)(38). La même étude a permis de réduire le risque d’exacerbations pulmonaires de 33% pour les patient·e·s asthmatiques et de tout de même 13% pour les patient·e·s avec BPCO (fig. 2B), le risque d’IVR ayant diminué de 33% resp. 50% (fig. 3B). Les études disponibles révèlent par ailleurs une bonne tolérance des lysats bactériens dans toutes les tranches d’âge. Sont actuellement en cours plusieurs vastes études cliniques randomisées centrées sur l’enfant, qui examinent spécifiquement la prévention primaire et secondaire de crises d’asthme et de wheezing ainsi que la suppression des infections récidivantes et du wheezing par des lysats bactériens(39,40).
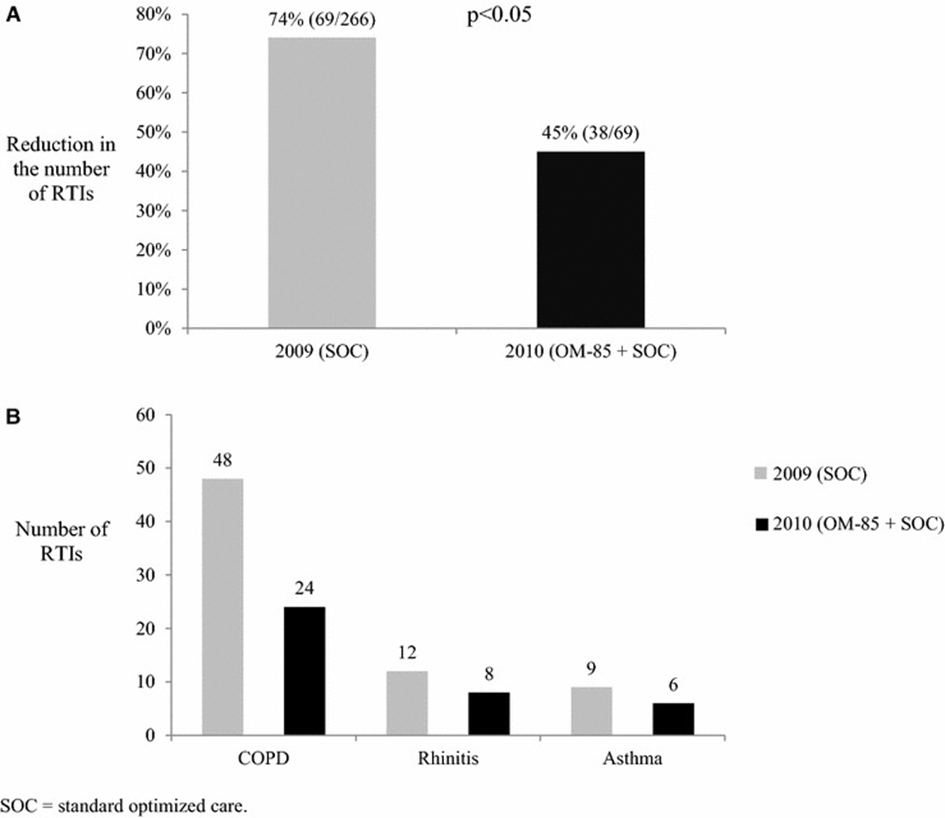
A. Diminution du nombre d’exacerbations pulmonaires en 2009 (vs 2008) et 2010 (vs 2009) par un lysat bactérien en plus du traitement standard(avec l’autorisation de 38).
B. Nombre d’exacerbations pulmonaires chez des patient·e·s avec BPCO, rhinite allergique et asthme en 2009 vs 2010.
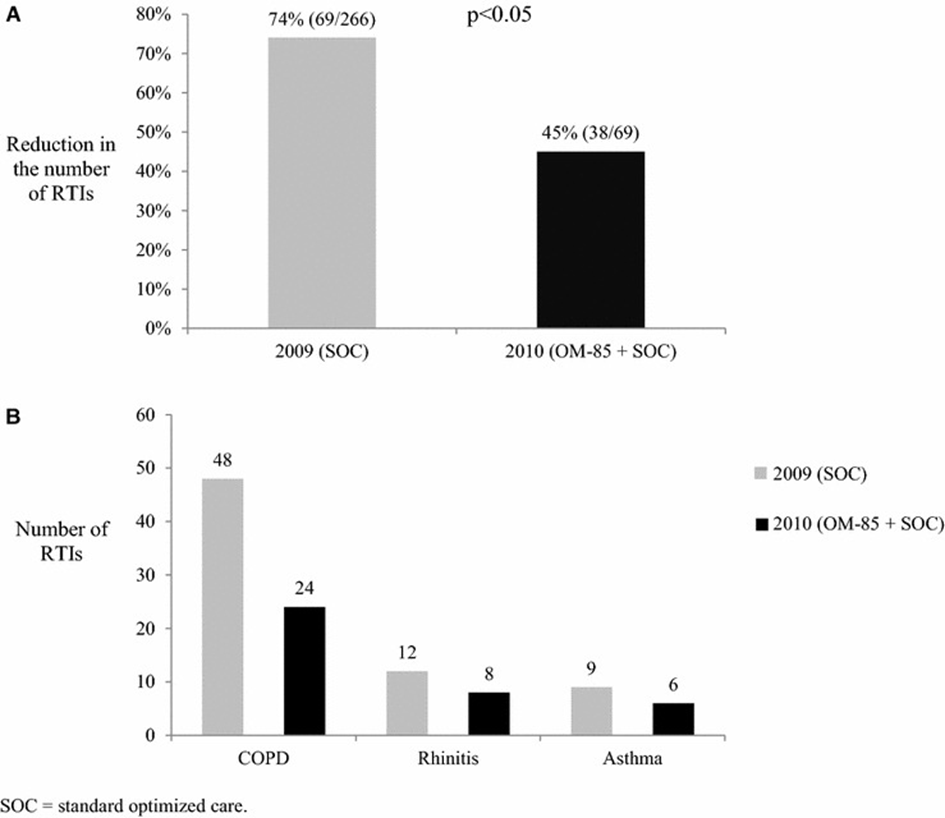
A. Diminution du nombre d’IVR en 2009 (vs 2008) et 2010 (vs 2009) par un lysat bactérien en plus du traitement standard(avec l’autorisation de 38).
B. Nombre d’IVR chez des patient·e·s avec BPCO, rhinite allergique et asthme en 2009 vs 2010.
Résumé et perspective
Dans de nombreuses situations cliniques il s’agit de diminuer la fréquence des infections virales des voies respiratoires, afin d’éviter des complications à long terme et préserver la qualité de vie. Dans ce contexte la prévention devient de plus en plus importante. Elle est notamment mieux comprise et acceptée depuis les expériences faites pendant la pandémie Covid-19. Toute mesure de prévention est donc bienvenue, que ce soient des masques pour des groupes à risque spécifiques, des vaccins et/ou l’immunomodulation, surtout par des lysats bactériens. Cela est d’autant plus vrai que les changements climatiques, la pollution de l’air et les allergies affectent fortement les voies respiratoires et que l’évolution future ne laisse, selon toutes les prévisions, guère place à l’optimisme. Dans ce contexte il faut mentionner deux études prospectives de cohortes qui suivent l’évolution de la santé pulmonaire d’enfants suisses en temps réel : BILD (Bern Basel Infant Lung Development)(41) et SPAC (Swiss Paediatric Airway Cohort)(19). Ces études pourront contribuer à mieux comprendre les facteurs de risque et à évaluer les mesures préventives à long terme.
Références
- Belachew AB, Rantala AK, Jaakkola MS, Hugg TT, Jaakkola JJ (2023). Asthma and respiratory infections from birth to young adulthood: The Espoo cohort study. Am J Epidemiol, 192(3):408-419.
- Romero-Tapia SDJ, Guzmán Priego CG, Del-Río-Navarro BE, Sánchez-Solis M (2023). Advances in the relationship between respiratory viruses and asthma. J Clin Med, 12(17):5501.
- Whittaker H, Nordon C, Rubino A, Morris T, Xu Y, De Nigris E et al. (2023). Frequency and severity of respiratory infections prior to COPD diagnosis and risk of subsequent postdiagnosis COPD exacerbations and mortality: EXACOS-UK health care data study. Thorax, 78(8):760-766.
- Edwards MR, Strong K, Cameron A, Walton RP, Jackson DJ, Johnston, SL (2017). Viral infections in allergy and immunology: how allergic inflammation influences viral infections and illness. J Allergy Clin Immunol, 140(4):909-920.
- Choi YI, Lee KS, Lee YS, Kim KR, Oh JW (2022). Analysis of the association among air pollutants, allergenic pollen, and respiratory virus infection of children in Guri, Korea during recent 5 Years. Allergy Asthma Immunol Res; 14(3):289-299.
- Endaryanto A, Darma A, Sundjaya T, Masita BM, Basrowi RW (2023). The notorious triumvirate in pediatric health: Air pollution, respiratory allergy, and infection. Children; 10(6):1067.
- Martinez FD (2016). Early-life origins of chronic obstructive pulmonary disease. New Engl J Med; 375(9):871-878.
- Svanes C, Sunyer J, Plana E, Dharmage S, Heinrich J, Jarvis D et al. (2010). Early life origins of chronic obstructive pulmonary disease. Thorax, 65(1):14-20.
- Gilles S, Blume C, Wimmer M, Damialis A, Meulenbroek L, Gökkaya M et al. (2020). Pollen exposure weakens innate defense against respiratory viruses. Allergy, 75(3):576-587.
- Hsu, AC, Parsons K, Barr I, Lowther S, Middleton D, Hansbro PM et al. (2012). Critical role of constitutive type I interferon response in bronchial epithelial cell to influenza infection. PloS One, 7(3):e32947.
- Dbouka T, Drikakisb D (2021). On pollen and airborne virus transmission. Phys. Fluids, 33:063313.
- Epstein TEG, Rorie AC, Ramon GD, Keswani A, Bernstein J, Codina R et al. (2025). Impact of climate change on aerobiology, rhinitis, and allergen immunotherapy: Work Group Report from the Aerobiology, Rhinitis, Rhinosinusitis & Ocular Allergy, and Immunotherapy, Allergen Standardization & Allergy Diagnostics Committees of the American Academy of Allergy, Asthma & Immunology. J Allergy Clin Immunol; S0091-6749(25)00268-4. doi: 10.1016/j.jaci.2025.01.048. Online ahead of print.
- Wan H, Winton HL, Soeller C, Tovey ER, Gruenert DC, Thompson, PJ et al. (1999). Der p1 facilitates transepithelial allergen delivery by disruption of tight junctions. J Clin Invest; 104(1):123-133.
- Monoson A, Schott E, Ard K, Kilburg-Basnyat B, Tighe RM, Pannu S et al. (2023). Air pollution and respiratory infections: The past, present, and future. Toxicol Sciences; 192(1):3-14.
- Hussey SJ, Purves J, Allcock N, Fernandes VE, Monks PS, Ketley JM, et al. (2017). Air pollution alters Staphylococcus aureus and Streptococcus pneumoniae biofilms, antibiotic tolerance and colonisation. Environment Microbiol, 19(5):1868-1880.
- Sun N, Ogulur I, Mitamura Y, Yazici D, Pat Y, Bu X et al. (2024). The epithelial barrier theory and its associated diseases. Allergy; 79(12):3192-3237.
- Holt PG, Upham JW, Sly PD (2017). Contemporaneous maturation of immunologic and respiratory functions during early childhood: implications for development of asthma prevention strategies. J Allergy Clin Immunol; 116(1):16-24.
- Damialis A, Gilles S, Sofiev M, Sofieva V, Kolek F, Bayr D et al. (2021). Higher airborne pollen concentrations correlated with increased SARS-CoV-2 infection rates, as evidenced from 31 countries across the globe. Proc Nat Acad Sciences; 118(12):e2019034118.
- Sundell N, Andersson LM, Brittain-Long R, Lindh M, Westin J (2016). A four year seasonal survey of the relationship between outdoor climate and epidemiology of viral respiratory tract infections in a temperate climate. J Clin Virol; 84:59-63.
- Gisler A, Eeftens M, de Hoogh K, Vienneau D, Salem Y, Yammine S et al. (2022). Pollen exposure is associated with risk of respiratory symptoms during the first year of life. Allergy; 77(12):3606-3616.
- Jones LL, Hashim A, McKeever T, Cook DG, Britton J, Leonardi-Bee J (2011). Parental and household smoking and the increased risk of bronchitis, bronchiolitis and other lower respiratory infections in infancy: systematic review and meta-analysis. Respir Res; 12(1):5.
- Chastin FM, Abaraogu U, Bourgois JG, Dall PM, Darnborough J, Duncan E et al. (2021). Effects of regular physical activity on the immune system, vaccination and risk of community-acquired infectious disease in the general population: Systematic review and meta-analysis. Sports Med 51(8):1673-1686.
- Hemilä H, Chalker E (2013). Vitamin C for preventing and treating the common cold. Cochrane Database Syst Rev; 2013(1):CD000980.
- Carboo JA, Dolman-Macleod RC, Malan L, Lombard MJ (2024). High-dose oral vitamin D supplementation for prevention of infections in children aged 0 to 59 months: a systematic review and meta-analysis. Nutr Rev; 82(5):579-599.
- Nault D, Machingo TA, Shipper AG, Antiporta DA, Hamel C, Nourouzpour S et al. (2024). Zinc for prevention and treatment of the common cold. Cochrane Database Syst Rev; 5(5):CD014914.
- Zhong K, Liu Z, Lu Y, Xu X (2021). Effects of yeast β-glucans for the prevention and treatment of upper respiratory tract infection in healthy subjects: a systematic review and meta-analysis. Eur J Nutr; 60(8):4175-4187.
- Vlassopoulou M, Yannakoulia M, Pletsa V, Zervakis GI, Kyriacou A (2021). Effects of fungal beta-glucans on health – a systematic review of randomized controlled trials. Food Funct; 12(8):3366-3380.
- Ballarini S, Ardusso L, Ortega Martell JA, Sacco O, Feleszko W, Rossi GA (2022). Can bacterial lysates be useful in prevention of viral respiratory infections in childhood? The results of experimental OM-85 studies. Front Pediatr; 10:1051079.
- Strickland DH, Judd S, Thomas JA, Larcombe AN, Sly PD, Holt PG (2011). Boosting airway T-regulatory cells by gastrointestinal stimulation as a strategy for asthma control. Mucos Immunol; 4(1):43-52.
- Pasquali C, Salami O, Taneja M, Gollwitzer ES, Trompette A, Pattaroni C et al. (2014). Enhanced mucosal antibody production and protection against respiratory infections following an orally administered bacterial extract. Front Med; 1:41.
- Dang AT, Pasquali C, Ludigs K, Guarda G (2017). OM-85 is an immunomodulator of interferon-β production and inflammasome activity. Scientific Reports; 7(1):43844.
- Pivniouk V, Gimenes-Junior JA, Ezeh P, Michael A, Pivniouk O, Hahn S et al. (2022). Airway administration of OM-85, a bacterial lysate, blocks experimental asthma by targeting dendritic cells and the epithelium/IL-33/ILC2 axis. J Allergy Clin Immunol; 149(3):943-956.
- Kaczynska A, Klosinska M, Janeczek K, Zarobkiewicz M, Emeryk A (2022). Promising immunomodulatory effects of bacterial lysates in allergic diseases. Front Immunol; 13:907149.
- Scott NM, Lauzon-Joset JF, Jones AC, Mincham KT, Troy NM, Leffler J et al (2017). Protection against maternal infection-associated fetal growth restriction: Proof-of-concept with a microbial-derived immunomodulator. Mucos Immunol; 10(3):789-801.
- Troy NM, Strickland D, Serralha M, de Jong E, Jones AC, Read J et al. (2022). Protection against severe infant lower respiratory tract infections by immune training: Mechanistic studies. J Allergy Clin Immunol; 150(1):93-103.
- Del‐Rio‐Navarro BE, Espinosa‐Rosales FJ, Flenady V, Sienra‐Monge JJ (2006). Cochrane Review: Immunostimulants for preventing respiratory tract infection in children. Cochrane Database Syst Rev; CD004974, doi: 10.1002/14651858.
- De Boer GM, Żółkiewicz J, Strzelec KP, Ruszczyński M, Hendriks RW, Braunstahl GJ et al. (2020). Bacterial lysate therapy for the prevention of wheezing episodes and asthma exacerbations: a systematic review and meta-analysis. European Respiratory Review; 29(158).
- Koatz AM, Coe NA, Cicerán A, Alter AJ (2016). Clinical and immunological benefits of OM-85 bacterial lysate in patients with allergic rhinitis, asthma, COPD and recurrent respiratory infections. Lung; 194:687-697.
- BEAR-Studie: OM-85 in paediatric recurrent respiratory tract infections with wheezing lower respiratory illness. ClinicalTrials.gov ID NCT05677763; https://clinicaltrials.gov/study/NCT05677763, letztmals aufgerufen 11.05.2025
- ORBEX-Studie: Oral bacterial extract for the prevention of wheezing lower respiratory tract illness. ClinicalTrials.gov ID NCT02148796; https://clinicaltrials.gov/study/NCT02148796, letztmals aufgerufen am 11.05.2025.
- Salem Y, Jakob J, Steinberg R, Gorlanova O, Fuchs O, Müller L et al. (2023). Cohort Profile Update: The Bern Basel Infant Lung Development Cohort. Int J Epidemiol; 53(1):dyad164. doi: 10.1093/ije/dyad164.
Informations complémentaires
Auteur·e·s
-
Dr. med. Andreas JungPädiatrische Pneumologie, Kantonsspital Winterthur, Zentrum für Kinder und Jugendliche, Winterthur
-
PD Dr. med. Oliver FuchsAllergologie, Zentrum Dermatologie und Allergologie, Departement Medizin, Luzerner Kantonsspital sowie Universität Luzern und Universität Bern
-
Dr. med. Philipp LatzinPädiatrische Pneumologie, Universitätskinderklinik Bern, Inselspital Bern, Universität Bern
-
Prof. Dr. med. Johannes WildhaberPädiatrie, Kantonspital Fribourg und Universität Fribourg, Fribourg
-
Prof. Dr. med. Nicolas RegameyPädiatrische Pneumologie, Kinderspital Zentralschweiz, Luzern und Pädiatrische Pneumologie, Universitatskinderklinik Bern, Inselspital Bern
